Трепонемные тесты на сифилис
Трепонемные тесты на сифилис. Общее описание.

Чтобы достоверно диагностировать сифилис и выявить противосифилитические антитела в организме больного (в сыворотке крови или спинномозговой жидкости), используют особые технологии лабораторных исследований — так называемые серологические методы.
При проведении диагностических тестов на сифилис, применяются различные серологические реакции: агглютинации, преципитации, иммунофлюоресценции, связывания комплемента, иммуноферментный анализ и др. В основе всех этих серологических реакций лежит взаимодействие антигенов и антител.
Специфические серологические тесты называются трепонемными потому, что в этих тестах используются бледные трепонемы или их антигены, то есть антигены трепонемного происхождения. Цель трепонемных тестов — выявление специфических антител к антигенным структурам возбудителя сифилиса, то есть антител, направленные конкретно против самих бактерий T. Pallidum, а не против тканей организма, поврежденных трепонемой. Специфические противотрепонемные антитела класса IgM могут быть обнаружены уже в конце второй недели заболевания.
Как и в нетрепонемных тестах, при проведении трепонемных тестов используется реакция "антиген-антитело". Для проведения и обнаружения результатов реакции "антиген-антитело" используют более сложные и дорогие методы, чем в случае нетрепонемных тестов.
Своевременное и качественное распознавание сифилитической инфекции связывается в настоящее время с широким внедрением трепонемных тестов.
Трепонемные тесты используют, чтобы подтвердить наличие сифилиса — с их помощью проверяют результаты нетрепонемных тестов, что особенно необходимо при диагностике скрытых форм сифилиса. Трепонемные тесты также применяются для выявления сифилиса на ранних стадиях, когда нетрепонемные кардиолипиновые тесты (реакция Вассермана, реакция микропреципитации и др.) отрицательные.
Трепонемные тесты применяются только для диагностики сифилиса и не используются для проведения контроля излеченности, т.к. трепонемные реакции у некоторых больных могут оставаться положительными в течение многих лет после полноценного лечения сифилиса.
Однако, при проведении трепонемных тестов, в небольшом числе исследований могут встречаться ложноположительные результаты, особенно при наличии у пациента таких заболеваний, как инфекционный мононуклеоз, болезни соедининтельной ткани, лепра или инъекционная наркомания.
По клинической специфичности трепонемные тесты сопоставимы с нетрепонемными, по клинической чувствительности – превосходят их.
Общие характеристики трепонемных тестов
На сегодняшний день предложено более 20 вариантов трепонемных специфических серологических тестов. При их проведении, в качестве антигена используют целые клетки или отдельные антигены T. pallidum штамма Nichols из яичка кролика, культуральные трепонемы или рекомбинантные белки бледной трепонемы.
При постановке трепонемных тестов применяются различные виды антигенов
- живые или фиксированные трепонемы;
- очищенные и обработанные ультразвуком трепонемы (соникат). Используются культуральные или (редко) патогенные штаммы T. Pallidum;
- специфические для T. pallidum биосинтетические или рекомбинантные антигены.
Трепонемные тесты имеют следующие общие характеристики:
- Применяется антиген трепонемного происхождения: используются либо подготовленные трепонемы, либо рекомбинантные белки – антигены возбудителя;
- В тестах определяются трепонемоспецифические антитела
- Методы - диагностические, подтверждающие, «золотой стандарт»
- Высокая чувствительность: чувствительность трепонемных тестов составляет от 70 до 100% в зависимости от вида теста и стадии сифилиса;
- Высокая специфичность: специфичность трепонемных тестов составляет 94 – 100%;
- Ложноположительные реакции при трепонемных тестах отмечаются реже, чем при нетрепонемных;
- «Надежность» при диагностике поздних форм сифилиса
Основными показаниями к применению трепонемных тестов для диагностики сифилиса являются:
- Проведение скрининга населения (используются методы ИФА, РПГА, простые быстрые тесты). Скрининг отдельных категорий населения на сифилис (доноров, беременных, больных офтальмологических, психоневрологических, кардиологических стационаров, ВИЧ-инфицированных).
- Подтверждение положительных результатов нетрепонемных тестов
- Тесты применяются для исключения ложноположительных результатов (ЛПР), ретроспективного подтверждения диагноза
- Подтверждение в случае расхождения результатов скринингового трепонемного теста и последующего нетрепонемного теста, а также скринингового и подтверждающего трепонемных тестов;
Ограничение применимости трепонемных тестов:
- трепонемные тесты не могут быть использованы для контроля эффективности терапии, т. к. антитрепонемные антитела длительно циркулируют в организме больного, перенесшего сифилитическую инфекцию;
- дают положительные результаты при невенерических трепонематозах и спирохетозах (боррелиоз, пинта, фрамбезия, беджель);
- могут давать ложноположительные реакции у больных с аутоиммунными заболеваниями, проказой, онкопатологией, эндокринной патологией и при некоторых других заболеваниях.
- трепонемные тесты дороже для проведения в расчете на одного больного, чем нетрепонемные тесты, поэтому возрастают затраты при проведении скрининговых обследований на сифилис
Трепонемные тесты на сифилис. Виды серологических реакций.
Наиболее известны следующие трепонемные тесты:
- Реакция связывания комплемента (реакция Вассермана) с трепонемным антигеном (РСКт).
- Реакция иммунофлюоресценции (РИФ; Fluorescent treponemal antibody, FTA). Она применяется в нескольких модификациях: РИФ-200 (FTA-200); РИФ-абс (FTA-abs; FTA-abs double staining; FTA-abs IgM; РИФ-абс-IgM; 19S-IgM-FTA-abs); РИФц — реакция иммунофлюоресценции с цельной кровью.
- Реакция пассивной гемагглютинации (РПГА; Treponema pallidum haemagglutination assay, TPHA).
- Реакция пассивной агглютинации желатиновых частиц, сенсибилизированных антигенами возбудителя сифилиса (TPPA, Treponema pallidum particle agglutination assay)
- Иммуноферментный анализ (ИФА; Enzyme Lynced Immunosorbent Assay, ELISA).
- ИХЛ — иммунохемилюминесцентное исследование (ИХЛ; Chemiluminescence immunoassays, CLIA)
- Реакция иммобилизации бледных трепонем РИБТ (РИТ), в зарубежной литературе TPI (Treponema pallidum immobilization test). В последние годы используется все реже и только в научных целях и в исследовательских лабораториях.
- Иммуноблотинг (ИБ; Western Blot, Line Blot). Как правило, используется метод линейного иммуноблотинга, являющийся вариантом иммуноферментного анализа. Применяется в двух вариантах: для выявления IgG и IgM-антител к возбудителю сифилиса
Реакция пассивной гемагглютинации (РПГА) и иммуноферментный анализ (ИФА) на антитела классов IgM, IgG и суммарные имеют универсальное значение и применяются как для скрининга, так и для подтверждения диагноза. Эти методики просты и доступны в проведении, имеют высокую воспроизводимость, автоматизированы. При применении ИФА или РПГА обязательным условием является использование в повторном анализе той же тест-системы, что и при первичном обследовании.
РИФ (fluorescent treponemal antibody, FTA) основана на визуализации при люминесцентной микроскопии комплексов антигенов с антителами с помощью сыворотки против Ig человека, меченной флюорохромом.
Методы РИФ, ИФА, иммуноблоттинг (ИБ) позволяют выявить специфические антитела к антигенам T. pallidum (при сифилисе результаты тестов становятся положительными) с 3-й недели от момента заражения и ранее, РПГА и РИБТ – с 7–8-й недели.
Из наиболее распространенных специфических трепонемных тестов в мировой практике, в которых используется реакция агглютинации, можно перечислить следующие. В РПГА (Treponema pallidum hemagglutination assay, ТРНА), реакции микрогемагглютинации (microhemagglutination assay for Treponema pallidum, MHA-TP) при положительном результате происходит агглютинация эритроцитов, сенсибилизированных (обработанных) трепонемным антигеном, в присутствии антитрепонемных антител. Использование в качестве носителя латекса или желатиновых частиц в тесте ТРРА (Treponema pallidum particle agglutination) позволяет применять нагрузочный тест в случае лизиса эритроцитов (распада эритроцитов из-за разрушения их мембраны) сыворотками некоторых больных, а также придает стабильность реагентам.
Трепонемные тесты
| Антиген | Улавливающая система | Тест |
|
Живые патогенные трепонемы
| Взвесь живых трепонем |
РИТ, РИБТ (реакция иммобилизации бледных трепонем)
|
| Интактные трепонемы | Трепонемы, фиксированные на стеклах |
РИФ (реакция иммунофлуоресценции), РИФ-абс (РИФ с абсорбцией), РИФ-ц, РИФ с капиллярной кровью из пальца и т.п.
|
| Очищенные и разрушенные ультразвуком трепонемы | Связаны с эритроцитами | РПГА (реакция пассивной гемагглютинации) |
| Связаны с желатиновыми частицами | Реакция агглютинации частиц (TPPA) | |
| Связаны с поверхностью лунок микропланшета | ИФА | |
|
Белки, разделенные методом электрофореза в полиакриламидном геле и перенесенные на мембраны методом вестерн-блоттинга
| Иммуноблоттинг | |
| Рекомбинантные | Связаны с поверхностью лунок микропланшета | Рекомбинантный ИФА |
|
Белки, разделенные методом электрофореза в полиакриламидном геле и перенесенные на мембраны методом вестерн-блоттинга
| Иммуноблотинг с рекомбинантными АГ | |
| Связаны с частицами латекса | Латекс-агглютинация |
РСКт - Реакция связывания комплемента с трепонемным антигеном (Реакция Вассермана)
1. Общее описание
В основе реакции Вассермана (РВ, RW) с трепонемным антигеном лежит реакция связывания комплемента (РСК; Complement Fixation Test, CFT). Трепонемный вариант теста принципиально отличаются по своим антигенам от классической реакции Вассермана, однако традиционно имеет то же название.
Модификации РВ, в которых использовались трепонемные антигены, были разработаны в конце 60-х годов. За рубежом РСК с протеиновой фракцией из патогенных и культуральных бледных трепонем вошла в практику как TPCF (Treponema pallidum complement fixation test) и RPCF (Reiter protein complement fixation test). В нашей стране Н.М.Овчинников и соавт. (1959) предложили применять для постановки РСК ультраозвученный трепонемный антиген из культуральных бледных трепонем, который в дальнейшем стал изготавливаться производственным путем.
Реакция Вассермана, которая широко используется и в настоящее время, обычно ставится с двумя или тремя антигенами. В качестве антигенов используются трепонемный антиген (убитые ультразвуком бледные трепонемы) и кардиолипиновый антиген (из сердца быка). В такой постановке РВ отличается более высокой чувствительностью, чем аналогичный нетрепонемный тест.
2. Принцип выполнения теста
Для постановки реакции параллельно используют кардиолипиновый и трепонемный антигены.
Кардиолипиновый антиген — это очищенный от балластных примесей спиртовый экстракт из мышц бычьего сердца, обогащенный холестерином и лецитином. Активность этого антигена обусловливается присутствием трех компонентов - фосфолипида, лецитина и холестерина. Так как составные компоненты (фосфолипин, лецитин) кардиолипинового антигена освобождены от балластных нейтральных жиров, этот антиген высоко чувствителен и достаточно специфичен. Кардиолипиновый антиген выпускается заводским образом.
Ультраозвученный трепонемный антиген приготовлен из нескольких штаммов культуральных бледных трепонем, отличающихся по своим антигенным свойствам и подвергнутых действию ультразвука. Этот антиген содержит протеиновый, полисахаридный и липоидный компоненты. Он также изготавливается предприятиями, занятыми в производстве биомедицинских препаратов и диагностических наборов.
Комплемент — группа белков, которые циркулируют в крови и являются частью иммунной системы. В РСКт в качестве комплемента применяют смесь сыворотки крови морских свинок, обработанной особым образом.
Реагины, находящиеся в сыворотке крови больных сифилисом, обладают свойством вступать в соединение с кардиолипиновым антигеном. Специфические антитрепонемные антитела вступают в соединение со специфическими трепонемными антигенами. Упомянутые антигены образуют совместно с антителами сыворотки крови больного иммунные комплексы «антиген-антитело», способные адсорбировать, связывать комплемент, вводимый в реакцию. Образованные комплексы (антитела + антигены + комплемент) невидимы, поэтому их индикация достигается введением гемолитической системы (смесь «гемолитическая сыворотка + эритроциты барана»).
Используемая в РВ гемолитическая сыворотка (гемолизин)— это сыворотка крови кролика или осла, иммунизированных эритроцитами барана. Гемолиз — это разрушение оболочки эритроцитов в результате чего гемоглобин выводится в окружающую эритроциты среду. Гемолизин — это вещество, вызывающее гемолиз.
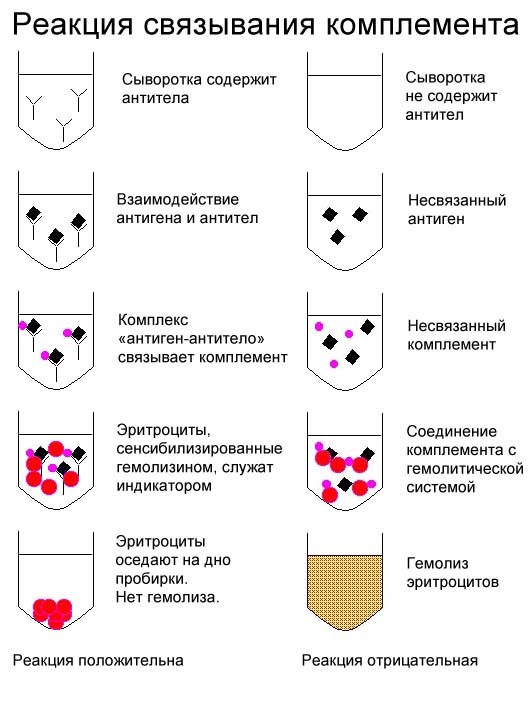
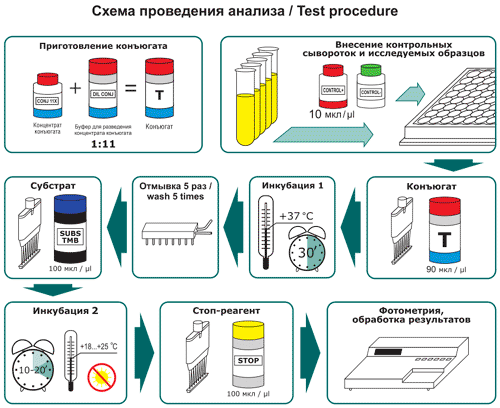
3. Постановка реакции Вассермана с трепонемным и кардиолипиновым антигеном
Исследование каждой испытуемой сыворотки крови проводят в трех пробирках с двумя антигенами. Одновременно исследуют для контроля заведомо положительные (4+, 2+) и отрицательную сыворотки крови.
РВ ставится в две фазы. В первую фазу, в пробирки с испытуемой инактивированной сывороткой крови (разведенной изотоническим раствором хлорида натрия) добавляют каждый из антигенов. В первую пробирку — добавляют трепонемный антиген, во вторую — разведенный кардиолипиновый антиген, а в третью контрольную — изотонический раствор хлорида натрия. Затем во все опытные и контрольные пробирки добавляют комплемент и проводят первичную 45-минутную инкубацию в термостате при 37°C.
Во вторую фазу во все пробирки добавляют гемолитическую систему (представляющую собой подготовленную особым образом смесь гемолитической сыворотки и эритроцитов барана). Содержимое пробирок перемешивают легким встряхиванием и помещают их в термостат при 37° на 45-50 минут до наступления полного гемолиза в контрольной пробирке.
Регистрируют результат реакции по наличию или отсутствию гемолиза в опытных пробирках.
Если комплемент связан в первой фазе реакции и образован комплекс «антитела + антиген + комплемент», то гемолиз не наступит. Эритроциты выпадут в осадок, легко заметный на дне пробирки невооруженным глазом. Это будет означать, что РВ положительная.
Если в испытуемой сыворотке нет противосифилитических антител, то комплемент не будет связан в первой фазе. Тогда он будет использован гемолитической системой и произойдет гемолиз. В пробирке – красная жидкость, без осадка. (РВ отрицательная).
4. Учет результатов
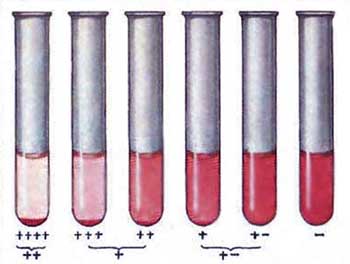
Для обозначения степени позитивности реакции Вассермана пользуются системой четырех плюсов (или крестов):
полная задержка гемолиза - 4+ (резко положительная реакция);
значительная задержка гемолиза - 3+ (положительная реакция);
частичная задержка гемолиза - 2+ (слабоположительная реакция);
незначительная задержка гемолиза - 1+;
сомнительная реакция - +/-.
Отрицательный результат реакции характеризуется полным гемолизом во всех пробирках опыта.
5. Специфичность и чувствительность
Специфичность реакции равна 98 %, чувствительность — 80 %
6. При каких стадиях заболевания лучше использовать
При первичном сифилисе РВ в большинстве случаев не имеет большого диагностического значения из-за малого процента положительных реакций у заболевших. Распознавание заболевания, как правило, проводят на основании клинических данных и исследования на бледную трепонему. В первые 15—17 дней после появления твердого шанкра РВ обычно отрицательная. В дальнейшем она переходит в положительную, причем процент положительных результатов возрастает с увеличением срока, прошедшего с начала появления шанкра до момента повторного исследования крови.
Реакция Вассермана с двумя антигенами становится положительной на 5–6-й неделе после заражения у 25–60 % больных, на 7–8-й неделе — у 75–96 %, на 9–16-й неделе — у 100 % пациентов. По мере развития сифилитической инфекции титр реагинов нарастает и достигает максимума (1:160–1:640 и выше) у больных вторичным свежим сифилисом, т. е. с давностью инфекции 9–12 недель.
Большое значение РВ имеет при выявлении подживших язв неясной этиологии, когда в большинстве случаев бледную трепонему найти не удается.
По мере «старения» инфекции титры антител снижаются, и у больных вторичным рецидивным сифилисом они не превышают 1:80–1:160.
При раннем скрытом сифилисе РВ положительная с высокими титрами антител (1:40–1:320 и выше) у 100 % больных, а при позднем скрытом сифилисе титры антител обычно не превышают 1:10– 1:20.
При вторичном сифилисе РВ положительна почти в 100 % случаев. Отрицательные результаты РВ при свежем нелеченном вторичном сифилисе наблюдаются очень редко. При вторичном рецидивном сифилисе РВ положительна в 98—100 % случаев. Следует отметить, что у истощенных лиц при так называемом злокачественном сифилисе и моносимптомных проявлениях вторичного рецидивного сифилиса РВ может быть отрицательной.
При третичном сифилисе РВ положительна у 70—75 % больных, с титрами антител, не превышающими 1:20–1:80. Поздние формы сифилиса внутренних органов и нервной системы проявляются положительными результатами РВ только у 50–80 % больных, а титры антител весьма вариабельны — от низких до высоких.
Наибольшее значение РВ имеет при скрытом сифилисе, так как какие-либо наружные проявления сифилиса в это время отсутствуют. В скрытом периоде сифилиса РВ бывает положительной в 40—96 % случаев в зависимости от длительности заболевания, интенсивности предшествующей терапии и т.д. Диагностическое значение имеют только положительные результаты реакции, отрицательные же роли не играют.
Большое значение проведение РВ имеет при сифилисе нервной системы. При этих заболеваниях необходимо проводить РВ не только с сывороткой крови, но и с цереброспинальной жидкостью и выполнять полное ее исследование. Сопоставление результатов РВ с сывороткой крови и цереброспинальной жидкостью может дать ценную информацию для дифференциальной диагностики. Так, при сифилисе головного мозга РВ с сывороткой крови положительна в 60—70 %, а с цереброспинальной жидкостью — примерно в 10 %, при прогрессивном параличе она положительна в обоих случаях почти в 100 % исследований.
При врожденном сифилисе РВ бывает положительной почти у 100 % детей с проявлениями раннего врожденного сифилиса и у 70—80 % — при позднем врожденном сифилисе.
Под влиянием лечения выраженность положительной РВ начинает быстро снижаться. Встречаются больные, у которых, несмотря на полноценное лечение, РВ остается резко положительной и после лечения. В таких случаях говорят о серорезистентности при сифилисе.
7. Ложноположительные и ложноотрицательные результаты
Положительные результаты РВ на сифилис у лиц, не страдающих этим заболеванием, называют ложноположительными. Частота ложноположительных результатов у здоровых лиц составляет 0,2—0,25 %. Если процент неспецифических ложноположительных результатов РВ у здоровых очень мал, то при некоторых заболеваниях он может быть высоким.
Все неспецифические результаты серологических реакций можно разделить на следующие основные группы:
1. Заболевания, обусловленные наличием общих антигенов у сходных возбудителей (спирохет): возвратный тиф, фрамбезия, беджель, пинта, трепонема полости рта, лептоспиры.
2. Положительные реакции, обусловленные изменением липидного обмена и изменением в глобулинах сыворотки. К ним относятся положительные результаты у беременных, больных подагрой, нарушения липидного состава в результате отравления свинцом, фосфором, после приема натрия салицилата, дигиталиса и др. В число этих реакций следует включить и положительные реакции при некоторых инфекционных заболеваниях (сыпной тиф, малярия, пневмония, лепра, эндокардит, коллагенозы, инфаркт миокарда, сотрясение мозга, онкологические заболевания, цирроз печени и др.)
3. Технические ошибки проведения. Неправильный выбор дозы комплемента, несоблюдение условий и сроков хранения реагентов, исключение из постановки реакции контрольных образцов сывороток крови, использование загрязненных пробирок и инструментов.
8. Модификация реакции Вассермана
Имеются модификации постановки реакции Вассермана в качественном и количественном вариантах, на холоде, со спинномозговой жидкостью.
Модификация РВ на холоде оказалась более чувствительной. Особенностью методики постановки реакции Вассермана на холоде является трехфазность температурных режимов, при которых протекает связывание комплемента. Эта реакция также ставится с кардиолипиновым и трепонемным антигеном.
Кроме качественной оценки РВ, имеется метод ее количественной постановки с различными разведениями сыворотки крови (1:10, 1:20, 1:80, 1:160, 1:320). Титр реагинов определяется максимальным разведением, еще дающим резко положительный результат (4+). Количественная постановка РВ имеет значение в диагностике некоторых форм сифилиса и при контроле за эффективностью терапии.
9. Область применения
В России РСКт входит в состав комплекса стандартных серологических реакций на сифилис (КСР).
Реакцию Вассермана с трепонемным и кардиолипиновым антигеном (РСКт) применяют для
- диагностики всех форм сифилиса,
- контроля за эффективностью лечения,
- обследования лиц, имевших половой контакт с больным сифилисом,
- обследования лиц с клиническим и анамнестическим подозрением на сифилис
- при профилактическом обследовании на сифилис больных психиатрических и неврологических стационаров, доноров и беременных, в том числе лиц, направляемых на искусственное прерывание беременности.
В настоящее время, приказом Министерства Здравоохранения РФ, рекомендовано заменить РСКт на более чувствительные трепонемные методы (ИФА или РПГА).
За рубежом реакция Вассермана с трепонемальным антигеном уже давно не применяется в клинической лабораторной практике и не входит в список стандартных тестов, рекомендованных Всемирной Организацией Здравоохранения.
Комплекс классических серологических реакций (КСР)
КСР - это комплекс реакций, применяемых для серодиагностики сифилиса в качестве стандартного метода. Этот комплекс реакций включает в себя реакцию Вассермана с кардиолипиновым антигеном (экстракт из сердца быка, обогащенный лецитином и холестерином) и трепонемным антигеном (обработанная ультразвуком взвесь апатогенных культуральных бледных трепонем ), а также микрореакцию преципитации (РМП) с плазмой или инактивированной сывороткой, которая ставится с кардиолипиновым антигеном
КСР становятся положительными в середине первичного периода (его деление на серонегативный и серопозитивный как раз и определяется по КСР), во вторичном периоде КСР положительны у 98-100% больных, а при третичном – лишь у 60- 70%. То есть, по мере увеличения давности заболевания позитивность КСР постепенно снижается.
Достоинства КСР:
1) Дешевизна, простота и быстрота постановки. Особенно это характерно для реакции микропреципитации: РМП в настоящее время – главный скрининговый (отборочный) метод;
2) Нетрепонемные тесты удобно использовать для контроля излеченности сифилиса.
Недостатки КСР:
1) Субъективность оценки результатов реакций («на глаз»);
2) Малая чувствительность при поздних формах сифилиса;
3) Недостаточная специфичность по сравнению с более современными тестами. При их проведении часто отмечаются ложноположительные реакции (ЛПР).
ЛПР могут быть обусловлены перекрестной реактивностью между бледной спирохетой и другими микробами, нарушениями липидного и белкового обмена, нестабильностью клеточных мембран, образованием аутоантител. ЛПР отмечаются при острых (малярия, инфекционный мононуклеоз и др.) и хронических (туберкулез, лепра, гепатит, боррелиоз и др.) инфекциях, инфаркте миокарда, циррозе печени, коллагенозах (особенно – при СКВ), онкопатологии, вакцинации, употреблении наркотиков, злоупотреблении алкоголем и жирной пищей. Ложноположительными могут быть КСР в последние недели беременности, после родов, а у некоторых женщин и во время месячных. Ложноотрицательные результаты КСР могут быть связаны с ВИЧ-инфекцией.
РИТ, РИБТ - Реакция иммобилизации бледных трепонем
Реакция иммобилизации бледных трепонем (РИБТ; Treponema pallidum immobilization test, TPI) — классический метод, который служит для выявления специфических трепонемных антител. Реакция РИБТ использует в качестве антигена патогенные бледные трепонемы T. pallidum (штамм Nichols), выращенные в яичке кролика. РИБТ основывается на потере подвижности живых бледных трепонем после воздействия антител из сыворотки крови пациента и комплемента. Результаты оцениваются посредством темнопольной микроскопии. Несмотря на то, что тест РИБТ был введен в клиническую практику в качестве специфического теста на сифилис, он является трудоемким, технически сложным, времязатратным и дорогим в применении.
1. История метода РИБТ
Реакция иммобилизации бледных трепонем (РИБТ) является фактически первым специфическим тестом для диагностики сифилиса. Эта реакция была представлена в 1949 году американскими исследователями Нельсоном и Майером (R. W. Nelson и M. M. Mayer) и подробно рассмотрена в научных работах в последующие десятилетия. Безуспешные попытки использовать живые трепонемы в тестах предпринимались и раньше. Благодаря тому, что Нельсону удалось создать среду, в которой трепонемы сохраняли жизнеспособность до 8 дней, его исследования увенчались успехом.
2. Принцип метода РИБТ
Метод основан на феномене потери бледными трепонемами подвижности в присутствии иммобилизирующих противотрепонемных антител исследуемой сыворотки крови и комплемента в анаэробных условиях. Антигеном служат живые патогенные бледные трепонемы, полученные от искуственно зараженных сифилисом кроликов.
3. Постановка теста РИБТ
В реакции участвуют испытуемая сыворотка, комплемент и антиген. К живым трепонемам, полученным из тканей яичка кролика после искусственного заражения, добавляют сыворотку крови исследуемого. При наличии в сыворотке противотрепонемных антител-иммобилизинов, бледные трепонемы прекращают движение (иммобилизируются). Антитела-иммобилизины относятся к поздним антитрепонемным антителам.
Реакция ставится с инактивированными прогреванием сыворотками или с образцами сывороток, высушенных на вощеной бумаге (сухие капли). Инактивацию сыворотки прогреванием проводят 30 минут при температуре 56°С. Перед взятием крови обследуемый не должен получать медикаменты, особенно препараты пенициллина. Прием препаратов отменяют на срок их возможной задержки в организме.
В качестве антигена используются бактерии штамма Никольса, полученные из 7–10-дневного кроличьего сифилитического орхита (воспаления яичка). Период от момента постановки реакции до регистрации ее результатов длится 18-20 часов, поэтому для сохранения жизнеспособности и хорошей подвижности микроорганизмов необходима среда выживания.
В РИБТ применяют комплемент морских свинок. Для получения комплемента кровь берут обязательно в условиях стерильности у нескольких морских свинок.
В случае бактериального загрязнения комплемент бракуют. Нельзя применять в реакции иммобилизации бледных трепонем консервированный комплемент, т.к. он токсичен для микроорганизмов.
В реакции иммобилизации используют избыток комплемента. Количество его в значительной степени зависит от среды выживания для бледных трепонем.
РИБТ ставят в стерильных боксах, предварительно облученных бактерицидной кварцевой лампой в течение 45-60 минут. Каждую сыворотку крови исследуют в двух пробирках: опытной и контрольной. В обе пробирки вносят исследуемую сыворотку и антиген в необходимых количествах. В опытную пробирку наливают активный комплемент, а в контрольную такое же количество инактивированной сыворотки крови морской свинки. После заполнения содержимое пробирок перемешивают легким встряхиванием.
РИБТ протекает в анаэробных условиях. Пробирки с ингредиентами помещают в микроанаэростат, из которого вакуумным насосом отсасывается атмосферный воздух и нагнетается газовая смесь из баллона (95 частей азота и 5 частей углекислого газа). Микроанаэростат с пробирками помещают в термостат (35°С) на 18-20 часов.
Оценку результатов РИБТ производят после извлечения пробирок из термостата и микроанаэростата (т.е. через 18-20 часов опыта). Пастеровской пипеткой на предметное стекло наносят каплю содержимого пробирки, которую накрывают покровным стеклом и исследуют в темном поле микроскопа (объектив 40, окуляр 10X). Просматривают несколько полей зрения в разных участках препарата, подсчитывая в каждом число подвижных и неподвижных бледных трепонем. Подсчет начинают с препарата из контрольной, а затем из опытной пробирки.
При постановке реакции применяют 5 контрольных исследований: с заведомо положительной и отрицательной сыворотками крови, с активным и инактивированным комплементом и средой выживания для бледных трепонем. Контрольную отрицательную сыворотку крови применяют для суждения о степени подвижности бледных трепонем в данном опыте. Контрольную положительную сыворотку крови - для оценки степени иммобилизирующей активности в условиях данного опыта. Исследование активного и инактивированного комплемента и среды проводят для определения их влияния на подвижность бледных трепонем.
При недостатке комплемента в опыте, иммобилизирующие антитела не проявляют свою активность должным образом и трепонемы остаются подвижными. Поэтому, после опыта проводят определение остаточного комплемента, чтобы оценить, не была ли подвижность бледных трепонем в опытных пробирках обусловлена отсутствием комплемента. Для этого применяется гемолитическая система — выдержанная в термостате смесь из взвеси эритроцитов барана и разведённой гемолитической сыворотки.
Остаточный комплемент определяют добавлением в каждую пробирку гемолитической системы в нужном объеме. Пробирки помещают в термостат при 37° на 45 минут. В опытных пробирках должен наступить гемолиз эритроцитов, в контрольных должна быть задержка гемолиза. Отсутствие в опытных пробирках гемолиза указывает на недостаточное количество комплемента, в этих случаях исследование надо повторить. Повторное исследование сыворотки крови не производят только в том случае, если отмечена 100% иммобилизация бледных трепонем.
4. Учет результатов РИБТ
Подсчет утративших подвижность, иммобилизованных трепонем ведется под микроскопом, методом темнопольной микроскопии. От исследователя требуется навык оценки движения трепонем. Ему следует обращать внимание на интенсивность движений, совершаемых бледной трепонемой. У этой бактерии не всегда можно наблюдать волнообразные сокращения и сгибательные движения, иногда только вращательные. Следует также уметь отличать активные движения трепонем от движения с током жидкости.
Для оценки результатов реакции рассчитывается процент иммобилизации бледных трепонем, т. е. соотношение подвижных и неподвижных трепонем в опыте (с активным комплементом) и контроле (с неактивным комплементом) по формуле:
X = (М – С)×100/М
где М — количество подвижных трепонем в контроле; С — количество подвижных трепонем в опыте; X — % иммобилизации. В практической работе процент иммобилизации определяют по заранее составленной таблице с применением вышеуказанной формулы.
Реакция иммобилизации бледных трепонем оценивается как
- положительная при иммобилизации 51 — 100% трепонем,
- слабоположительная: 31 — 50% неподвижных трепонем,
- сомнительная: 21 — 30% неподвижных трепонем,
- отрицательная: 0 — 20% неподвижных трепонем.
5. При каких периодах заболевания лучше использовать
Реакция иммобилизации бледных трепонем становится положительной в конце первичного – начале вторичного периода сифилиса (с 7—8-й недели от момента заражения и более). Вместе с тем РИБТ малопригодна для диагностики ранних стадий сифилиса, поскольку антитела, иммобилизирующие бледные трепонемы и определяемые в реакции, появляются только через 3-6 недель после заражения. Антитела-иммобилизины относятся к классу иммуноглобулинов IgG. Они появляются в крови позже реагинов (антикардиолипиновых антител), позже антител-флюоресцинов (выявляются РИФ и ИФА) и преципитинов (выявляются РМП).
В дальнейшем РИБТ остается положительной. Отмечается высокая чувствительность реакции при поздних формах сифилиса. При вторичном, позднем сифилисе, нейросифилисе, врожденном сифилисе положительный результат РИБТ регистрируется в 95–100 % случаев. При третичном сифилисе, при специфических поражениях внутренних органов, нервной системы, когда РВ часто отрицательная, РИБТ дает положительные результаты в 98 — 100% случаев.
6. Чувствительность и специфичность
РИБТ долгое время признавалась самым специфичным тестом на сифилис. По данным литературы, специфичность РИБТ равна 99 %, чувствительность колеблется от 79 до 94 %. По данным ЦНИКВИ, чувствительность РИБТ (суммарно, по всем стадиям сифилиса) составляет 87,7%.
7. Область применения метода
Сфера применения РИБТ постепенно сужается из-за длительности постановки, дороговизны и трудоемкости. РИБТ — это достаточно сложный и затратный анализ, требующий высокой квалификации персонала и наличия вивария. В связи с этим применение данного метода в последние годы существенно сократилось. В США этот тест в настоящее время применяется только в исследовательских лабораториях.
Исходя из сложности и дороговизны РИФ и РИБТ, имеет смысл применять их для диагностики поздних и скрытых форм сифилиса. РИБТ сохраняет свои позиции как «реакция-арбитр» при дифференциальной диагностике ранних скрытых форм сифилиса и ложноположительных результатов. Эта реакция может быть полезн при диагностике нейросифилиса и при расхождении результатов других серологических тестов.
РИБТ становится положительной значительно позже, чем РИФ и РВ. Поэтому для диагностики заразных форм сифилиса она не применяется.
РИБТ, как и РИФ, очень медленно негативируется в процессе противосифилитической терапии. Вследствие этого она непригодна для контроля за ходом противосифилитической терапии.
8. Источники и причины ошибок при постановке, ложноположительные и ложноотрицательные результаты
Ложноположительные результаты (ЛПР) при РИБТ редки и отмечены главным образом при ряде трепонематозов (фрамбезия, пинта, беджель), не встречающихся в России, а также при лепре, саркоидозе, СКВ, туберкулезе, циррозе печени и некоторых других редких заболеваниях несифилитической природы. С возрастом пациентов число ложноположительных результатов РИБТ увеличивается.
РИБТ может оказаться ложноположительной, если в исследуемой сыворотке содержатся трепонемоцидные вещества (например, пенициллины, тетрациклины, эритромицин), вызывающие неспецифическую иммобилизацию бледных трепонем, Это может быть следствием приема трепонемоцидных антибиотиков пациентом, поэтому обследование не проводят лицам, получавшим антибиотики в течение последнего месяца. Кровь на РИБТ можно исследовать не ранее 2 недель после окончания приема антибиотиков и других противосифилитических препаратов.
9. Модификации реакции иммобилизации бледных трепонем
Помимо микроанаэростатной методики существует меланжерная постановка РИБТ по Н.М. Овчинникову. Анаэробные условия при постановке реакции создаются помещением реагирующей смеси в меланжер (лейкоцитарный смеситель), оба конца которого закрыты резиновым кольцом. Меланжерная методика реакции позволяет обходиться без вакуумного насоса, баллона со смесью азота и углекислого газа, микроанаэростата. При сравнительном изучении на большом клиническом материале получены результаты, не уступающие классической анаэростатной методике.
10. Особенности, преимущества и недостатки РИБТ
РИБТ — это технически сложный и дорогостоящий метод диагностики. Технология требует значительных средств для содержания кроликов и проведения тестирования. Этот трудоемкий тест в настоящее время он применяется в основном для научных целей. В большинстве зарубежных стран уже почти 40 лет РИБТ практически используется не для диагностических целей, а только в научно-исследовательской работе.
Недостатки реакции:
- РИБТ требует работы с живыми патогенными бледными трепонемами штамма Никольс, остающегося заразным для человека несмотря на адаптацию для кроликов
- постановка реакции сложна, трудоемка и дорогостояща
- необходимо наличия вивария
- требуется высококвалифицированный персонал для постановки реакции, учета результатов и содержания вивария
- субъективность оценки результатов
- отсутствие автоматизации
- нет возможности стандартизировать этот серологический метод.
- реакция неприменима на фоне проводимой антисифилитической терапии
- невозможность использовать для контроля излеченности. РИБТ у больных сифилисом может оставаться положительной в течении многих лет (и даже – пожизненно), несмотря на полученное полноценное лечение.
- реакция может давать ложноположительные результаты у больных злокачественными опухолями, диабетом, лепрой, аутоиммунными заболеваниями, пневмонией, тяжелой сердечно-сосудистой патологией.
Достоинствами РИБТ являются:
1) Достаточно высокая чувствительность;
2) Высокая специфичность.
РИФ (Реакция иммунофлюоресценции)
Реакция иммунофлюоресценции (РИФ) - метод экспресс-диагностики для выявления антигенов микробов или определения антител. Тесты, основанные на детекции флюоресцентного сигнала, считаются одними из лучших тестов на сифилис.
1. История метода
Трепонемный флюоресцентный тест — реакция иммунофлюоресценции — РИФ (Fluorescent treponemal antibody, FTA) был впервые разработан в 1957 г. Deacon и соавторами (Deacon, Falcone and Harris).
2. Принцип метода
Метод РИФ основан на том, что антигены тканей или микробы, обработанные иммунными сыворотками с антителами, меченными флюорохромами, способны светиться в УФ-лучах люминесцентного микроскопа. Бактерии в мазке, обработанные такой люминесцирующей сывороткой, светятся по периферии клетки в виде каймы зеленого цвета
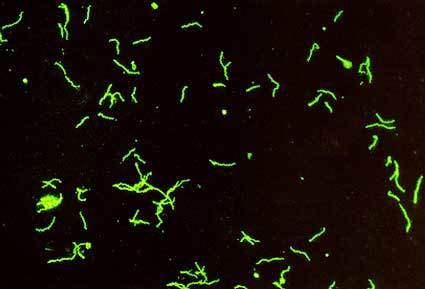
В качестве антигена в РИФ используется взвесь живых патогенных бледных трепонем штамма Никольс из орхита кролика, которая высушивается на предметном стекле и фиксируется ацетоном. К высушенным и фиксированным ацетоном к стеклу бледным трепонемам добавляется сыворотка крови больного.
После промывания препарат обрабатывается сывороткой, содержащей антитела против иммуноглобулинов человека, меченные флюоресцином. Еще раз промывают препарат и смотрят его под люминесцентным микроскопом. Если в исследуемой сыворотке есть противотрепонемные антитела-флюоресцины, будет отмечаться желто-зеленое свечение трепонем.
3. Способ проведения исследований методом РИФ
Фиксированный на предметном стекле антиген (патогенные бледные трепонемы) обрабатывается испытуемой сывороткой. После промывания препарат обрабатывается люминесцентной сывороткой против иммуноглобулинов человека, меченной флюорохромом. При этом образующийся флюоресцирующий комплекс (античеловеческий глобулин + флюоресцеин тиоизоционат) связывается с человеческим глобулином на поверхности бледной трепонемы, обеспечивая свечение бледной трепонемы под люминесцентным микроскопом.
Для выявления комплексов антиген-антитело применяют люминесцирующую сыворотку, представляющую конъюгированные с ФИТЦ антивидовые (противочеловеческие) иммуноглобулины. Наличие в сыворотке антител к трепонемам определяют по свечению трепонем при исследовании в люминесцентном микроскопе. Тест проводят в качественном и полуколичественном вариантах.
4. Учет результатов
Визуализация результатов РИФ проводится с помощью люминесцентного микроскопа. Результаты оцениваются по степени свечения трепонем в препарате. При наличии антител видно свечение трепонем, если же в сыворотке не было противотрепонемных антител, то трепонемы не видны. Степень свечения фиксированных к стеклу высушенных бледных трепонем обозначаются в «плюсах» (от «–» до «++++»). Отрицательный результат — отсутствие свечения или уровень фона — 1+.
5. При каких периодах заболевания лучше использовать
Реакция иммунофлюоресценции (РИФ) достаточно чувствительна на всех стадиях инфекции, с окончания периода инкубации до позднего сифилиса. Первичный период сифилиса при классическом течении начинается через 3-4 недели после заражения. РИФ становится положительной в первые дни первичного периода или даже в конце инкубационного периода, с 3-й недели после инфицирования. Результаты РИФ остаются положительными во всех периодах, в том числе при поздних формах.
РИФ становится положительной несколько раньше, чем РВ. По некоторым данным, положительная РИФ бывает у 80% больных первичным серонегативным сифилисом. Во вторичном периоде РИФ положительная почти в 100% случаев. Она всегда положительная при латентном сифилисе и дает 95 — 100% положительных результатов при поздних формах заболевания и врожденном сифилисе.
6. Чувствительность и специфичность
Реакция иммунофлюоресценции (РИФ) – это группа методов, обладающих высокой чувствительностью и специфичностью. РИФ чувствительна во всех стадиях инфекции, начиная от периода инкубации и заканчивая поздним сифилисом. По данным ВОЗ, чувствительность РИФ при первичном сифилисе – 70-100%, при вторичном и позднем – 96–100%, специфичность – 94–100%. По данным ЦНИКВИ, чувствительность РИФ при всех формах сифилиса составляет 99,1%.
Специфичность РИФ может быть повышена путем предварительной обработки исследуемой сыворотки сорбентом — ультраозвученным трепонемным антигеном, связывающим групповые антитела (РИФ-абс).
7. Область применения метода
РИФ применяется:
- как подтверждающая реакция при раннем, скрытом сифилисе
- при установлении ретроспективного диагноза
- для дифференциации скрытых форм сифилиса и ложноположительных результатов исследований на сифилис.
- как подтверждающий тест при нейросифилисе.
РИФ достаточно широко используют в качестве подтверждающего теста, но она не предназначена для рутинного использования или скрининга, поскольку в техническом отношении трудна для постановки. Для выполнения РИФ необходимо наличие вивария или приобретение взвеси патогенных бледных трепонем, что ограничивает возможности реакции. Однако в последние годы на отечественном рынке начали появляться тест-системы, позволяющие проводить реакцию при отсутствии вивария и собственного лабораторного штамма патогенных бледных трепонем.
8. Источники и причины ошибок при постановке, ложноположительные и ложноотрицательные результаты
ЛПР при постановке РИФ бывают редко (при коллагенозах, боррелиозе).
9. Особенности, преимущества и недостатки
РИФ до сих пор считают одним из лучших тестов на сифилис, «золотым стандартом» серодиагностики. РИФ в сравнении с РИБТ более проста в постановке,
Несмотря на высокую диагностическую ценность, широкому внедрению РИФ в повседневную практику препятствуют необходимость использования живой T. pallidum, высокая стоимость и длительность проведения исследования. Постановка реакции трудоемка. Кроме того, оценка результатов РИФ носит субъективный характер.
Достоинствами РИФ и РИБТ являются:
1) Высокая чувствительность (особенно для РИФ);
2) Высокая специфичность (особенно для РИБТ).
Недостатки РИФ и РИБТ:
1) Техническая сложность, дороговизна методов.
2) Субъективность оценки результатов, отсутствие автоматизации;
3) РИФ и РИБТ у больных сифилисом могут оставаться положительными в течении многих лет (и даже – пожизненно), несмотря на полученное полноценное лечение. Поэтому эти реакции невозможно использовать для контроля излеченности.
10. Модификации метода
На практике для серодиагностики сифилиса используется и использовалось несколько модификаций реакции иммунофлюоресценции:
- РИФ-абс – наиболее чувствительный метод серодиагностики сифилиса, становится позитивным раньше других реакций (с 3-ей недели от заражения);
- РИФ-200 (сыворотка пациента при постановке разводится в 200 раз) – высоко специфичный метод серодиагностики сифилиса.
- РИФ-10 (разведение испытуемой сыворотке в 10 раз) - более чувствительный метод, чем РИФ-200.
- РИФ-ц проводят с ликвором.
- РИФ-абс-IgM - выявление ранних противотрепонемных антител класса IgM.
1. Наибольшее распространение получила модификация РИФ-абс — реакция иммунофлюоресценции с абсорбцией. Перед постановкой реакции сыворотка обследуемого истощается смесью непатогенных трепонем для исключения перекрестных реакций. Групповые антитела удаляются из исследуемой сыворотки с помощью разрушенных ультразвуком культуральных трепонем, что существенно повышает специфичность реакции. Поскольку исследуемая сыворотка используется в разведении 1:5, то РИФ-абс отличается высокой чувствительностью.
РИФ-абс рекомендуется для ранней серодиагностики сифилиса, так как она становится положительной уже на третьей неделе после заражения, т. е. за несколько дней до появления шанкра или одновременно с ним.
Основными показаниями для использования РИФ-абс в клинической практике являются:
- диагностика скрытых и поздних форм сифилиса,
- выявление ложноположительных результатов КСР и РМП, особенно у беременных и соматических больных при подозрении на сифилис,
- для установления ретроспективного диагноза заболевания.
РИФ-абс мало информативна при оценке результатов лечения: у 85 % больных, получивших адекватную противосифилитическую терапию, положительные результаты РИФ сохраняются многие годы.
Эту реакцию называют «золотым стандартом» серодиагностики сифилиса. Ее используют для арбитражных случаев, но для достоверного результата необходима свежая концентрированная взвесь T. pallidum штамма Nichols из семидневного орхита у кролика, которую нельзя замораживать.
2. В СССР ставилась в двух модификациях — РИФ-10 и РИФ-200, т. е. с разведением испытуемой сыворотки в 10 и 200 раз. РИФ-200 — исследуемая сыворотка разводится в 200 раз для уменьшения количества ложноположительных результатов. Это обеспечивает высокую специфичность реакции, но чувствительность ее несколько падает. РИФ-10 более чувствительна, но чаще дает неспецифические положительные результаты, чем РИФ-200, отличающаяся высокой специфичностью. РИФ-10 более чувствительна, РИФ-200 и РИФ-абс – более специфичны.
Чувствительность РИФ-200 и РИФ-абс оценивается 84–99 %, а специфичность — 97–99 %.
3. РИФ-ц проводят с ликвором. Реакция ставится с использованием цельной спинномозговой жидкости для выявления специфических поражений ЦНС.
4. Реакция РИФ-абс-IgM предложена для выявления ранних противотрепонемных антител класса IgM. Эта реакция может использоваться для диагностики врожденного сифилиса, ранних форм сифилиса и дифференциальной диагностики случаев реинфекции и серорецидива.
Известны 2 модификации этой реакции:
– FTA-ABS-IgM, основанная на использовании во второй фазе реакции конъюгата анти-IgM (меченные флюоресцеином антитела к IgM человека) вместо античеловеческого флюоресцирующего глобулина;
– российский вариант РИФ-абс-IgM, отличающийся тем, что к исследуемой сыворотке крови добавляется сорбент, удаляющий IgG-антитела, а с оставшимися IgM-антителами ставится РИФ-абс.
Основными показаниями к постановке РИФ-абс-IgM являются:
– серодиагностика врожденного сифилиса при отсутствии у ребенка манифестных проявлений врожденного сифилиса на коже и слизистых оболочках;
– дифференциальная диагностика реинфекции и клинико-серологического или серологического рецидива сифилиса, при котором РИФ-абс-IgM будет отрицательной, а РИФ-абс — положительной;
– оценка эффективности терапии раннего приобретенного или врожденного сифилиса: после адекватного лечения РИФ-абс-IgM становится отрицательной в течение ближайших 3–6 месяцев.
Эта реакция может использоваться для выявления врожденного сифилиса. Известно, что крупные молекулы IgM не могут проходить через здоровую плаценту. Следовательно, антитела класса М против бледной трепонемы могут появиться в организме ребенка или вследствие нарушения барьерной функции плаценты или же они вырабатываются организмом ребенка, больного сифилисом. Антитела класса IgM появляются в крови больного сифилисом уже в первые недели болезни, а антитела класса IgG появляются позже. Раздельное определение антител обоих классов оказывается исключительно полезным при диагностике врожденного сифилиса у детей, так как наличие у ребенка на первом месяце жизни антител класса IgM будет указывать, что они образованы организмом больного сифилисом ребенка, в то время как выявление только антител IgG будет говорить о материнском происхождении последних.
Постановка реакции 19S(IgM)-РИФ-абс предполагает предварительное разделение c помощью гель-фильтрации более крупных молекул 19S IgM от
фракции более мелких молекул 7S IgG. Дальнейшее исследование в реакции РИФ-абс сыворотки крови, содержащей только фракцию 19S IgM,
устраняет все возможные источники ошибок. Но техника постановки этой реакции сложная и трудоемкая, требует специального оборудования и подготовки специалистов.
Реакция иммунного прилипания (РИП, TPIA — Treponema pallida immunoadherence).
Эта реакция основана на использовании феномена, который в 1912 г. описал Rieckenberg. РИП основана на том, что вирулентные тканевые трепонемы, сенсибилизированные сывороткой больного сифилисом, в присутствии комплемента и эритроцитов прилипают к поверхности эритроцитов и при центрифугировании увлекаются с ними в осадок, исчезая из надосадочной жидкости.
Для постановки реакции используются следующие ингредиенты: испытуемая сыворотка, антиген, комплемент, эритроциты донора, изотонический раствор натрия хлорида. В качестве антигена используют взвесь бледных трепонем штамма Никольса.
Наиболее широко применительно к серодиагностике сифилиса этот тест изучался отечественными и зарубежными авторами в 50—60-е годы. Данные о ценности РИП как диагностического теста были противоречивы. Реакция требовала максимальной точности, так как при неточном разливе ингредиентов, при избытке или недостатке исследуемого материала в препарате получались недостоверные результаты.
В России обширные исследования провела Л.В. Сазонова, которая получила близкие результаты в РИП и РИТ при использовании свежеприготовленной взвеси патогенных бледных трепонем штамма Никольса. Однако применение прогретого или консервированного фенолом антигена резко искажало результаты реакции и делало антиген нестабильным. Рекомендовать данный тест для замены РИТ Л.В. Сазонова сочла невозможным.
Г.П. Авдеева, применив при изготовлении антигена другие температурный и временной режимы, получила при изучении РИП иные результаты. По ее данным, чувствительность этой реакции выше чувствительности KCP и РИТ, но несколько уступает РИФ, а специфичность РИП, РИТ и РИФ близка.
Однако отсутствие производственного выпуска антигена для РИП не позволило более широко изучить этот тест и внедрить его в практику.
РПГА-реакция пассивной гемагглютинации
Реакция пассивной гемагглютинации (РПГА) является распространенным серологическим тестом, прочно укоренившимся в лабораторной практике. обладает достаточно высоким уровнем эффективности при исследовании.
1. История метода РПГА
Впервые о применении РПГА для диагностики сифилиса сообщили G.Blumental и W.Bachman (1932). В 1965 г, для диагностики сифилиса была предложена реакция непрямой, или пассивной, гемагглютинации. О модификации реакции с использованием различных антигенов сообщалось Ratlev Т. в 1965 — 1967 гг. Микромодификацию РПГА предложили Сох Р.М. и соавторы в 1969 году. Первую коммерческую тест-систему разработали японские ученые Tomisava et. al. в 1969 г.
2. Принцип метода РПГА
Из подготовленной однородной взвеси эритроцитов, «нагруженных» антигенами, при добавлении исследуемой сыворотки, содержащей антитела, выпадает осадок в виде хлопьев. Полученный осадок состоит из эритроцитов, "склеенных" антителами, и называется «гемагглютинат». Взвесь эритроцитов подготавливается заранее и поставляется в составе диагностических тест-систем.
Процесс склеивания эритроцитов, на поверхности которых присутствуют антигены, называется «гемагглютинация». Склеивание происходит под действием специфических антител (агглютининов). Реакция называется «пассивной», т.к. собственные антигены эритроцитов не вступают в реакцию, а сами эритроциты выполняют исключительно вспомогательную индикаторную функцию.
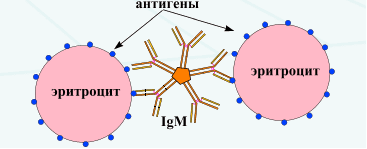
Реакция пассивной (непрямой) гемагглютинации — это разновидность реакции агглютинации, в которой в качестве носителей антигенов используются именно эритроциты (от греч. háima — кровь), а не другие частицы. В общем случае, в реакции агглютинации под действием антител происходит склеивание и выпадение в осадок микробов или других клеток — не обязательно эритроцитов, а, например частиц латекса, бактерий или других антигеннесущих корпускулярных частиц.
При реакции пассивной гемагглютинации для диагностики сифилиса, в качестве антигена используются эритроциты барана или птиц, покрытые антигенами бледных трепонем. При добавлении сыворотки, содержащей специфические антитела, происходит склеивание эритроцитов (агглютинация).
Реакцию РПГА относят к иммунологическим методам, т.к. она основана на специфическом взаимодействии антигена патогенной бледной трепонемы с антителом. В соответствии с «теорие решетки» агглютинация является результатом «сшивки» поверхностных молекул антигена молекулами антител (иммуноглобулинов).
3. Постановка реакции пассивной гемагглютинации
РПГА ставят в пластиковых планшетах или в пробирках с разведениями сыворотки крови больного, к которым добавляют эритроцитарный диагностикум.
Процесс соединения антигена с эритроцитами называют сенсибилизацией, а полученный таким образом искусственный корпускулярный антиген — сенсибилизированными эритроцитами. Эритроцитарными диагностикумами называются эритроциты, сенсибилизированные антигеном.
Для приготовления диагностикума применяют обработанные вначале формалином, затем танином эритроциты барана или птиц (чаще куриные), которые подвергают сенсибилизации ультра-озвученным антигеном патогенной бледной трепонемы (штамм Никольса) или рекомбинантными белками бледной трепонемы (TpN15, TpN17, TpN47). Также могут использоваться эритроциты барана, сенсибилизированных ультраозвученным антигеном культуральных бледных трепонем.
Исследуется только сыворотка (не использовать плазму крови) . Не подходят гемолизированные и мутные образцы. Отрицательным контролем служат несенсибилизированные эритроциты (для исключения наличия антиэритроцитарных антител). В каждой серии постановок используют положительный и отрицательный контроль.
В лунки (ячейки) иммунологического планшета вносят образцы исследуемой сыворотки крови и тест-эритроциты. Если в сыворотке крови пациента содержатся специфические противотрепонемные антитела, то при добавлении исследуемой сыворотки в лунку с антигеном происходит образование комплексов "антиген-антитело", связанных с поверхностью носителей (эритроцитов). Визуально это проявляется склеиванием эритроцитов, т. е. гемагглютинацией, которая видна невооруженным глазом. Иммунные комплексы "антитело-антиген-эритроцит", которые под действием сил тяжести постепенно опускаются вниз, распределяются по всей поверхности дна лунки и формируют характерную картину «перевернутого зонтика».
В зависимости от количества антител, содержащихся в исследуемом образце, изображение «перевернутого зонтика» варьируется от максимального, занимающего всю поверхность дна лунки, до небольшого участка в центральной, самой низко расположенной его части (с просветлением в центре и формированием более интенсивного кольца из осевших эритроцитов по периферии).
Иммунные комплексы не образуются, если в образце нет специфических антител или при добавлении в реакцию контрольных (интактных) эритроцитов. При этом, эритроциты постепенно собираются в самой нижней точке дна лунки, формируя фигуру в виде компактного пятна или «пуговки», иногда с незначительным просветлением в центре.
Если сыворотка крови человека содержит антиэритроцитарные антитела, то «зонтик» сформируется в любом случае — как в реакции с тест-эритроцитами, так и с контрольными эритроцитами. В этом случае для выявления специфических антитрепонемных антител рекомендуют применять другие медицинские технологии.
Возможен феномен прозоны (невозможность реакции из-за избытка антител), устраняемый разведением сыворотки.
4. Учет результатов реакции пассивной гемагглютинации
Результаты РПГА учитывают визуально через 60—120 минут при постановке микрометода и через 2–4 ч или на следующий день при постановке макроварианта. При использовании более крупных (ядросодержащих) эритроцитов птиц получают более четкую картину, учет результатов проводят в более ранние сроки.
Возможно определение титра (высокий титр РПГА ≥ 1:2 560).
Результаты исследования оцениваются по 4+ системе (от «–» до «++++») по величине образовавшейся пленочки. При появлении агглютинации эритроциты располагаются на поверхности лунки в виде «зонтика», а при отрицательном результате эритроциты свободно соскальзывают вниз и скапливаются на дне в центре лунки в виде «пуговки».
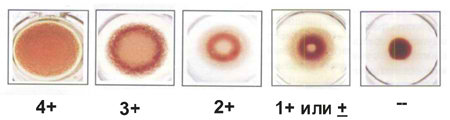
Общепринятая оценка результатов РПГА:
4+ — положительная РПГА. Агглютинированные эритроциты в виде «зонтика» равномерно выстилают всю поверхность лунки;
3+ — положительная РПГА. Эритроциты выстилают всю поверхность лунки, но часть их «соскальзывает» к центру. При этом по периферии осадка формируется заметное кольцо;
2+ — слабоположительная РПГА. Эритроциты образуют пленку на небольшом участке нижней части лунки, формируя плотное кольцо из осадка эритроцитов с заметным просветлением в центре;
1+ — неопределенная РПГА, эритроциты образуют рыхлый осадок на дне лунки с нечеткими краями и незначительным просветом в центре;
(–) — отрицательная РПГА, все эритроциты лежат на дне лунки в виде компактного осадка («пуговки» или колечка) на чистом окружающем фоне (без окружающего зернистогоосаждения).
В зарубежной практике результаты РПГА также оценивают как реактивные (в случае образования агглютината), слабореактивные (если образования незначительны) и нереактивные (если не наблюдается агглютинации).
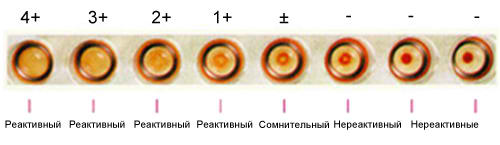
Учет результатов реакции может производиться автоматически с применением специальных анализаторов. Помимо качественного исследования, во всех тест-системах предусмотрен количественный анализ с определением титра.
5. При каких периодах заболевания лучше использовать РПГА
РПГА становится положительной в середине первичного периода (7-8 недель от момента заражения, через 3–4 недели после появления твердого шанкра ) и после лечения годами сохраняется положительной.
При очень высоком уровне антител к трепонеме в исследуемой сыворотке (что наиболее характерно для вторичного сифилиса) возможен ложноотрицательный результат РПГА (так называемый феномен «прозоны»).
Специфические антитела-агглютинины выявляются в крови переболевших сифилисом людей в течение длительного времени, поэтому РПГА не может быть рекомендована для дифференциальной диагностики реинфекции или определения остроты инфекционного процесса.
РПГА не применяется для контроля излеченности, т.к. может оставаться положительной спустя много лет после выздоровления. Вместе с тем ее можно использовать как дополнительный (к РМП или к RPR) метод при контроле эффективности проведенного лечения, исследуя динамику снижения титров антител. Обязательным условием при этом является использование той же РПГА тест-системы, что и при первом (до лечения) обследовании пациента, а также проведение исследования в той же лаборатории.
6. Чувствительность и специфичность РПГА
РПГА считается высокочувствительным и специфичным тестом. Эта реакция является ценным диагностическим тестом при всех формах сифилиса, но особенно чувствительна она при поздних формах заболевания. В зависимости от стадии заболевания чувствительность РПГА колеблется. При первичном сифилисе чувствительность РПГА составляет 76% (и выше), при вторичном сифилисе – до 100%. При скрытом раннем — 97 %, при позднем сифилисе — 94 %, со специфичностью 98–100%. Более низкая чувствительность при свежих формах заболевания объясняется более поздним формированием агглютининов.
По данным ГУ «ЦНИКВИ Росздрава» чувствительность РПГА при диагностике различных форм сифилиса составила 99,4%. Большинство исследователей отмечают 98-99% специфичность РПГА.
По чувствительности и специфичности РПГА не уступает, а при поздних формах и врожденном сифилисе даже превосходит РИФ и РИБТ.
7. Область применения метода РПГА
РПГА может применяться в качестве как скринингового, так и подтверждающего теста; может быть использована в полуколичественном варианте с расчетом титра антител. Разработаны количественный метод постановки РПГА, микрометод, а также автоматизированная реакция микрогемагглютинации.
8. Особенности, преимущества и недостатки РПГА
По данным литературы, РПГА стабильно заняла лидирующее место в клинической практике в большинстве стран мира. РПГА – наиболее широко используемый тест в клиниках ИППП за рубежом.
Методика РПГА проста в выполнении, не требует специального оборудования: для ее постановки нужен лишь планшет для гемагглютинации. Исследование не занимает длительного времени; реакция высоко чувствительна и специфична. Апробация метода в клинической практике показала, что он является исключительно простым, дешевым и чувствительным. Как и ИФА, РПГА проста в исполнении, не требует высокой квалификации персонала и специального оборудования, возможна ее автоматизация.
Преимущества РПГА-теста:
- простой в постановке и интерпретации,
- не требует специального оборудования,
- время получения результата – 45 минут,
- пригоден для массового скрининга (необходимо всего 25 мкл сыворотки в разведении 1:20),
- высокая степень стандартизации,
- наличие внутренних контролей,
- большой срок годности,
- приемлемая цена
- возможность автоматизации учета.
Следует отметить также недостатки РПГА:
- возможность неспецифических реакций при наличии антиэритроцитарных антител,
- отсутствие корреляции титра и стадии сифилиса,
- более поздняя позитивация реакции на ранних стадиях сифилиса,
- возможность ложноположительных реакций у лиц, принимавших алкоголь, наркоманов,
- чувствительность к вибрации и температуре в лаборатории.
Преимуществами РПГА по сравнению с РИБТ и РИФ являются:
- использование промышленных тест-систем,
- возможность автоматизации реакции,
- нет необходимости работать с живой бледной трепонемой,
- отпадает потребность в виварии.
9. Источники и причины ошибок при постановке РПГА, ложноположительные и ложноотрицательные результаты
Реакция пассивной гемагглютинации является относительно несложным исследованием; при ее выполнении необходимо соблюдать все рекомендации производителей диагностикума и правила работы в клинико-диагностической лаборатории. Допущенные ошибки могут приводить к появлению и регистрации как ложноотрицательных, так и ложноположительных результатов реакции. Ложноположительные результаты РПГА могут быть обусловлены влиянием человеческого фактора и факторов биологической природы.
Ложноположительные результаты могут быть получены
- при исследовании сывороток крови пациентов с невенерическими трепонематозами,
- за счет ревматоидного фактора
- за счет перекрестно реагирующих с трепонемным антигеном антител, образующихся при различных системных или индуцированных лекарствами и наркотиками нарушениях обмена,
- из-за аномального уровня иммуноглобулинов;
- у новорожденных детей - за счет образования в организме плода или ребенка IgM-антител к IgG матери, что осложняет трактовку результатов и диагностику врожденного сифилиса.
Ошибки, вызванные влиянием фактора участия человека на исследование:
- загрязненные микропланшеты
- неправильное пипетирование
- наличие вибрации в лаборатории
- температура воздуха в лаборатории выходит за диапазон температуры: 18–25 градусов
К наиболее типичным техническим ошибкам при постановке РПГА, приводящим к получению недостоверных результатов, следует отнести:
- неточное разведение ингредиентов,
- нарушение температурного режима,
- нарушение времени инкубации реагентов,
- нарушение сроков нанесения реагентов на планшет,
- несоответствие рН растворов требуемым,
- загрязнение лабораторной посуды.
Источником ошибок при постановке РПГА могут являться и следующие технические моменты:
- исследование в реакции гиперлипидемичной, гемолизированной сыворотки крови или образцов с признаками бактериального пророста;
- исключение из постановки реакции контрольных сывороток крови;
- неравномерная концентрация эритроцитов в диагностикуме вследствие недостаточного его перемешивания перед использованием;
- нарушение сроков и условий хранения диагностикума и контрольных эритроцитов; использование наборов с истекшим сроком годности;
- использование при постановке реакций загрязненных пробирок, наконечников пипеточных дозаторов, пипеток, иммунологических планшетов, растворов;
- неточности при первичном разведении образца сыворотки крови;
- недостаточная тщательность выполнения последовательных двукратных разведений;
- несоблюдение температурного режима и времени инкубации;
- наличие посторонних вибраций и встряхиваний иммунологического планшета во время инкубации;
- нарушение методики постановки РПГА, выражающееся в отказе от выполнения исследования с контрольными эритроцитами.
Применение плазмы крови, содержащей антикоагулянты, способные вызывать неспецифическую агглютинацию эритроцитов (РПГА), может привести к получению результатов, не подлежащих трактовке.
Число ложноположительных и ложноотрицательных результатов меньше, чем при других серологических тестах. ЛПР при постановке РПГА бывают редко и возможны при трепонематозах (фрамбезия, беджель, пинта). Также, ложноположительные результаты регистрировались (в сумме менее 1 %) у наркоманов, у больных инфекционным мононуклеозом, боррелиозом, лепрой, при коллагенозах, циррозе печени, лимфосаркоме, а также у беременных.
Ложноотрицательные результаты реакции могут быть обусловлены конкуренцией между IgM- и IgG-антителами. Также ложноотрицательные результаты возможны у ВИЧ-инфицированных пациентов.
10. Модификации метода РПГА
Существует микро- и макромодификации постановки РПГА, чаще используется первая из-за экономичности, быстроты постановки и учета результатов.
Кроме того, разработан автоматический диагностический комплекс анализа изображений, что позволило производить количественную автоматическую оценку результатов и исключить субъективизм в интерпретации полученных данных. Аппаратно-программный комплекс распознает изображение, проводит обработку данных и выдает ответ в относительных единицах.
Для автоматизации учета результатов РПГА также используются ридеры и автоматические анализаторы.
ТРРА (Treponema pallidum particle agglutination) - реакция агглютинации искусственных частиц для выявления антител к Treponema pallidum
Краткое описание теста TPPA
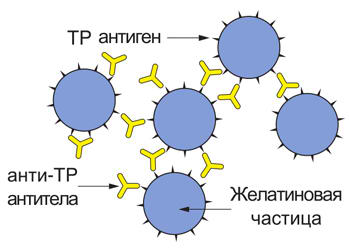
В настоящее время для диагностики сифилиса применяют также модификацию метода пассивной гемагглютинации — ТРРА (Treponema pallidum particle agglutination), в которой антиген бледных трепонем фиксирован на желатиновых частицах. Так как на искусственных полимерных частицах нет собственных антигенов, обусловливающих биологическую активность, то наборы для серодиагностики сифилиса на их основе имеют основания считаться более совершенными. Использование биологически инертных искусственных частиц сводит к минимуму неспецифическую агглютинацию, обычно наблюдаемую при использовании других носителей.
TPPA используется для серологической диагностики антител к различным видам и подвидам патогенных трепонем. Этот тест может использоваться для определения антител к возбудителям сифилиса, пинты, беджеля и фрамбезии.
Процедура исследования весьма проста и не требует специального оборудования — используются стандартные «U»-образные микропланшеты. В основе теста лежит агглютинация желатиновых частиц, сенсибилизированных антигенами T. pallidum, антителами, содержащимися в сыворотке крови пациента.
TPPA — это подтверждающий трепонемный тест, который удобно использовать как для исследования малого числа образцов, так и для массового скрининга. TPPA используется за рубежом в качестве подтверждающего теста и для замены микро-гемагглютинационного теста MHA-TP (microhemagglutination assay for antibodies to T. pallidum).
Чувствительность теста TPPA составляет от 85% до 100%, а специфичность — от 98% до 100%. Чувствительность TPPA для первичного сифилиса - 88%, для вторичного и позднего скрытого сифилиса 98%-100%.
Если TPPA используется для диагностики сифилиса, то антитела к другим видам трепонем (таким, как T. pallidum endemicum, pertenue, или carateum) могут вызвать ложноположительные результаты. Существует ряд методов, позволяющих удалить эти антитела из сывороточных образцов перед началом теста.
Принцип теста TPPA
TPPA — это метод пассивной агглютинации желатиновых частиц в сыворотке или плазме крови человека. Сыворотка, содержащая антитела к патогенной трепонеме, реагирует с желатиновыми частицами, сенсибилизированными антигеном бледных трепонем штамма Никольса, подвергнутых действию ультразвука. В результате реакции, в лунке планшета для микротитрования формируется гладкая пленка агглютинированных желатиновых частиц.
Если антитела отсутствуют, то частицы оседают на дно лунки планшета, формируя компактную «пуговку» из неагглютинированных частиц. Контрольные лунки с несенсибилизированными желатиновыми частицами должны также показать такую компактную «пуговку» для каждой сыворотки, то есть отсутствие агглютинации.
Содержащиеся в тест-наборах желатиновые частицы дополнительно окрашиваются.
Применение теста TPPA
ТРРА — это тест универсального назначения, который может одинаково успешно применяться как при обязательном профилактическом обследовании групп населения на сифилис (скрининге), так и в специализированных дерматовенерологических учреждениях. Достоинством теста TPPA является его высокая чувствительность, не уступающая классическим тестам, которые до недавнего времени являлись «золотым стандартом» серодиагностики сифилиса. Среди других достоинств теста — высокая воспроизводимость, а также простота и скорость постановки реакции.
Тест TPPA применяется для подтверждения положительных результатов нетрепонемных скрининговых тестов на сифилис, таких, как тест VDRL, а также для обследования пациентов с отрицательными результатаи нетрепонемных тестов, но имеющих признаки или симптомы, указывающие на поздний сифилис. Не рекомендуется использование TPPA в качестве единственного скринингового теста на сифилис.
Кроме того, агглютинационный тест ТРРА может использоваться для исследования образцов спинномозговой жидкости при диагностике нейросифилиса. При этом, как и в отношении других серологических тестов, интерпретация результатов должна проводиться при обязательном сочетании с другими показателями и симптомами заболевания.
Результаты теста TPPA
Оценка результата происходит по системе «плюсов» — от (–) до (2+). Результаты теста видны невооруженным глазом и интерпретируются следующим образом:
| Степень агглютинации | Показатель теста | Интерпретация |
|---|---|---|
| Агглютинированные частицы равномерно выстилают дно лунки планшета | 2+ | Положительный |
| Достоверное большое кольцо с неровными внешними полями и периферической агглютинацией | 1+ | Положительный |
| Частицы образуют компактное кольцо с просветом в центре и плавными гладкими
внешними границами | ± | Слабоположительный |
| Частицы формируют в центре лунки компактное кольцо с незначительным просветом в центре и ровной внешней границей | – | Отрицательный |
| Частицы формируют в центре лунки «пуговку» с ровной внешней границей | – | Отрицательный |

Учет результатов производят, чтобы определить соответствие описанию выше. Образцы, показавшие неопределенный результат (±) необходимо исследовать повторно. В случае, если в нескольких тестах методом TPPA образец показывает неопределенный результат, рекомендуется провести исследование с помощью других методов.
Результаты анализа не следует рассматривать изолированно. Например, на ранней стадии инфекции число антител ещё слишком незначительно, вследствие чего TPPA и многим другим методам не хватает чувствительности. Поэтому, в случае подозрения на сифилис, даже если результаты тестов отрицательны, образцы необходимо исследовать ещё раз. Для постановки диагноза необходимо учитывать клинические симптомы, имеющиеся у пациента, клиническую историю и другие данные.
Так же, как и в реакции РПГА, для TPPA может наблюдаться феномен прозоны и ложноотрицательный результат в случае, если образец сыворотки содержит слишком высокий титр антител.
ИФА - Иммуноферментный анализ
Иммуноферментный анализ (ИФА; The enzyme linked immunosorbent assay, ELISA) является одним из многочисленных методов серологической диагностики инфекционных заболеваний. Иммуноферментный анализ (ИФА) в серодиагностике сифилиса — это тест на антитела классов M, G и A (IgM, IgG, IgA) против антигенов бледной трепонемы. Возможна постановка ИФА с ликвором.
Внедрение в практику иммуноферментного анализа (ИФА) вместо реакции Вассермана и других кардиолипиновых тестов значительно повысило качество лабораторной диагностики сифилиса. Существенным преимуществом данного метода является возможность автоматизации процесса исследования, что позволяет снизить влияние человеческого фактора.
1. История метода ИФА
Основные принципы иммуноферментного анализа на поверхности твердофазного носителя разработали E.Engvar и соавтор. (1971), B.Van Weeman и A.Schuurs (1971). Разработанный ими иммуноферментный анализ впервые был предложен для диагностики сифилиса в 1975 г. J. Veldkamp и A. Visser, которые оценили потенциал этого автоматизированного теста. ИФА начал повсеместно использоваться в диагностике сифилиса в 1980-е гг., когда были разработаны и сертифицированы диагностические тесты и стандартизированы методики тестирования. В СССР методику постановки ИФА для диагностики сифилиса разработали B.Н.Беднова, А.В.Бабий и А.В.Котровский (1982, 1983).
2. Принцип метода ИФА
Иммуноферментный анализ (ИФА) по механизму реакции близок к РИФ (выявляются те же антитела). Реакцию иммуноферментного исследования относят к иммунологическим реакциям, основанным на высокоспецифическом взаимодействии антигенов бледной трепонемы с антителами больного сифилисом.
В сифилидологической практике используется в основном непрямой вариант ИФА. Принцип наиболее часто используемого непрямого варианта реакции состоит в следующем. На поверхности лунок полистиролового планшета фиксируются иммунные комплексы, образующиеся при взаимодействии антител больного сифилисом с антигенами бледной трепонемы. После этого их выявляют их в цветной реакции с помощью специфических коньюгатов и соответствующих субстратно-хромогенных добавок.
Порядок выполнения теста следующий: на твердофазный носитель с присоединенным к нему антигеном помещается сыворотка больного. При наличии в ней антител, на поверхности носителя образуется комплекс антиген-антитело. Для «проявления» результатов реакции используются антивидовые антитела к Ig человека, конъюгированные с ферментными маркерами. В случае положительной реакции фермент, присоединившийся к комплексу антиген-антитело, разлагает добавленный в систему субстрат, в результате чего развивается цветное окрашивание разной интенсивности.
В реакции определения комплекса сорбированных на твердой фазе АГ и АТ проводят с помощью антиглобулиновых антител, меченных ферментом, по цветной реакции фермента с субстратом.
В реакции определение комплекса сорбированных на твердой фазе антигенов и антител проводят с помощью антиглобулиновых антител, меченных ферментом.
ИФА представляет возможность выявления сывороточных Ig разных классов. На рынке представлены системы, позволяющие определять раздельно IgM и IgG и суммарные антитела.
Специфические антигены, применяемые для ИФА, могут иметь различное происхождение:
• ультраозвученные — их получают при результате разрушения бактериальной клетки T.pallidum ультразвуком или иным методом;
• рекомбинантные — их получают генно-инженерными технологиями путем внедрения в геном бактериальной клетки (например, кишечной палочки E.Coli) гена, ответственного за синтез определенного антигена T.pallidum, с последующим наращиванием бактериальной массы продуцирующего микроорганизма, разрушением этих клеток, выделением и очисткой антигена;
• пептидные — получают в результате последовательного химического синтеза антигенных эпитопов белков T.pallidum.
Организм способен образовать антитела почти к любой части молекулы антигена. При нормальном иммунном ответе этого обычно не происходит. Один или несколько иммуногенных пептидов, выделенных из белкового антигена обладают особой антигенностью, и большинство антител образуется именно к ним. На них развивается наиболее интенсивный иммунный ответ. Наибольшую информативность в ИФА показали иммунодоминантные участки белков бледной трепонемы с молекулярной массой 15 кД, 17кД и 47кД. В качестве антигена использовали детергентный экстракт, или соникат патогенных трепонем штамма Никольс.
3. Способ проведения исследований методом
Принцип метода заключается в выявлении сорбированного на твердой фазе (поверхность лунок пластикового планшета) специфического комплекса антиген-антитело антиглобулиновыми антителами, меченными ферментом (пероксидазой), с помощью цветной реакции с субстратом, учитываемой количественно спектрофотометрически.
Антигены, применяемые для сенсибилизации лунок полистиролового планшета могут быть:
- лизатными — полученными в результате разрушения ультразвуком бледной трепонемы;
- пептидными — полученными в результате химического синтеза фрагментов белков бледной трепонемы и имеющими антигенную реактивность, аналогичную исходным белкам возбудителя;
- рекомбинантными — полученными с помощью методов генной инженерии, несущими антигенные детерминанты, идентичные бледной трепонеме.
В сифилидологической практике обычно используется непрямой вариант ИФА.
4. Учет результатов
При ИФА для визуализации реакции антиген-антитело используют реакцию фермента (щелочная фосфатаза или пероксидаза хрена) с субстратом, который при этом меняет свою окраску. Интенсивность окраски определяет позитивность реакции (от «–» до «++++»). Результаты ИФА могут оцениваться визуально по 4-бальной системе или инструментально в виде цифровых показателей оптической плотности, получаемых на специальных ридерах (типа Мультискан) при длине волны 492 нм. Т.к. оценка результатов проводится спектрофотометрически, это исключает субъективную интерпретацию.
5. При каких периодах заболевания лучше использовать
Сроки позитивации ИФА - с 4-ей недели от заражения. Результаты ИФА (как и РИФ) становятся положительными в первые дни первичного периода или в конце инкубации и остаются положительными во всех периодах. ИФА особенно ценен в ранней диагностике сифилиса – положительные результаты выявления антител могут быть получены уже в конце инкубационного периода заболевания (т. е. на 4–6-й неделе после инфицирования).
6. Чувствительность и специфичность
ИФА – высокочувствительный и специфичный тест, что является его преимуществом. ИФА по механизму реакции, чувствительности и специфичности близок к РИФ, т.к. в обеих реакциях принимают участие одни и те же антитела. Большинство исследователей отмечают высокую специфичность и чувствительность на всех стадиях болезни. Чувствительность различных вариантов ИФА, по данным Г. А. Дмитриева, достигает 98–100 %, а специфичность — 96–100 %. По данным ЦНИКВИ, чувствительность ИФА при сифилисе составляет 99,1% (Приказ № 87 М3 РФ).
Вариант твердофазного ИФА (enzyme-linked immunosorbent assay, ELISA) относится к самым чувствительным серологическим реакциям, позволяя выявлять 0,0005 мкг/мл антител и 0,000005 мкг/мл антигенов.
7. Область применения метода
Метод рекомендуется использовать при обследовании беременных, контактных лиц, доноров и представителей групп риска. ИФА может применяться как в качестве скринингового, так и подтверждающего теста. За относительно короткое время своей истории, ИФА превратился из ориентировочного теста в подтверждающий. В диагностике сифилиса тест используется также как подтверждающий для образцов, демонстрирующих положительные результаты при использовании различных нетрепонемных тестов и РПГА.
Метод ИФА может быть использован в количественном варианте с расчетом индекса позитивности, или реактивности, который позволяет оценивать уровень антител в образце.
В настоящее время в России применение иммуноферментного анализа для диагностики сифилиса регламентировано Приказом Минздрава РФ №87 от 26 марта 2001 года «О совершенствовании серологической диагностики сифилиса» (приложение №1 «Постановка отборочных и диагностических тестов на сифилис»). В приказе планируется замена РСК в комплексе серореакций (КСР) на ИФА и РПГА.
8. Источники и причины ошибок при постановке, ложноположительные и ложноотрицательные результаты
Иммуноферментный анализ является сложным многоступенчатым исследованием, при котором необходимо строго соблюдать все рекомендации производителей диагностических наборов, правила регулировки и настройки применяемой в исследовании аппаратуры.
Источником ошибок при постановке ИФА могут являться следующие моменты:
• исследование в реакции гиперлипидемичной, гемолизированной сыворотки крови или образцов с признаками бактериального пророста;
• не практиковать двух- и более кратного замораживания образца биологического матери¬ала, при необходимости повторного исследования использовать сыворотку из пробирки-дубликата;
• нарушение сроков и условий хранения иммуносорбента и отмывающего раствора; использование тест-наборов с истекшим сроком годности;
• применение компонентов реакции из других диагностических наборов;
• нарушение времени проведения этапов реакции;
• высыхание лунок иммунологического планшета на этапах реакции;
• повторное использование пластиковой посуды (пластиковых лоточков) для приготовления смеси хромогена и субстрата;
• несоблюдение периодичности метрологического контроля параметров работы применяемых аппаратов (вошера и спектрофотометра);
• использование при постановке реакций загрязненной лабораторной посуды: колб, мерных цилиндров, пробирок, пипеток, наконечников пипеточных дозаторов;
• недостаточная тщательность выполнения разведений образцов биологического материала;
• ошибки при внесении образца биологического материала в соответствующую лунку планшета;
• ошибки при перенесении результатов исследования в журнал регистрации, протокол исследования или бланк ответа.
Тщательное выполнение рекомендаций инструкций по применению диагностических тест-наборов, регулярная поверка точности пипеточных дозаторов и автоматических приборов, применение внутреннего положительного и отрицательного контролей позволяют получать результаты ИФА-исследования с высокой воспроизводимостью.
9. Особенности, преимущества и недостатки
ИФА относится к современным, перспективным методам серодиагностики сифилиса ввиду его простоты, воспроизводимости, доступности. Определение антител методом ИФА является идеальным способом диагностики, подходящим для одновременного исследования большого числа образцов. Благодаря своим преимуществам, он завоевал популярность во всех странах.
Технология ИФА-исследования предусматривает соблюдение всех рекомендаций производителей коммерческих диагностических тест-наборов и тщательности выполнения процедуры исследования. Для проведения исследований в ИФА необходимо приобретение дополнительного специального оборудования. Методика постановки занимает более длительное время по сравнению с РМП, RPR и РПГА.
Наличие автоматизации ряда этапов или всего процесса в целом позволяет одновременно исследовать большое количество образцов биологического материала при высокой степени стандартизации исследования, минимизации субъективного элемента в оценке результатов, возможности хранения фиксированных протоколов исследования, что позволяет архивировать данные исследования и обращаться к ним повторно для ретроспективного анализа.
Достоинства:
- Дает возможность дифференцированного и суммарного определения IgM и IgG антител к возбудителю сифилиса.
- высокая чувствительность и специфичность, приближающиеся к 100%,
- воспроизводимость
- возможности автоматизации
К преимуществам ИФА относят высокую специфичность (96-100%) и чувствительность (98-100%), отмечаемые большинством исследователей.
Наличие автоматизации ряда этапов или всего процесса в целом позволяет одновременно исследовать поток с большим количеством образцов биологического материала при высокой степени стандартизации исследования, минимизации субъективного элемента в оценке результатов, возможности хранения фиксированных протоколов исследования, позволяющих архивировать данные исследования и обращаться к ним повторно для ретроспективного анализа.
Существенными недостатками методик, выполняемых вручную, в т. ч. определения антител к антигенам T. pallidum методом ИФА, являются:
~ возможные ошибки персонала при проведении исследования (оплошность, небрежность, нарушение технологии);
~ невозможность полной стандартизации процесса исследования при ручном варианте постановки ИФА;
~ повышенный риск заражения персонала.
10. Модификации метода
Наряду с классическим непрямым ИФА известен и метод ловушечного ИФА. Он был предложен в 1989 г. O. E. Ijsselmudien и соавт. для выявления антител класса IgM к антигенам Tr. pallidum. Метод обладает высокой специфичностью и чувствительностью.
На поверхности лунок планшета сорбированы очищенные антитела к иммуноглобулинам человека класса M, и после инкубации исследуемой сыворотки все IgM связываются с носителем. Наличие же среди связанных IgM специфичных для антигенов Tr. pallidum выявляется с помощью антигенов Tr. pallidum, конъюгированных с ферментом.
Этот метод позволяет выявлять антитела не только класса IgM, но и классов IgG, IgA. Для этого лунки планшетов сенсибилизируются аффинно очищенными антителами определенного класса против иммуноглобулинов человека. При этом из сыворотки вылавливаются антитела этого класса, а выявление трепонемоспецифических антител осуществляется путем их соединения с конъюгатом, представляющих соединение трепонемного антигена с ферментом.
Использование ловушечного варианта иммуноферментного анализа снижает риск ложноположительных реакций, опосредованных ревматоидным фактором крови, перекрестными реакциями между иммуноглобулинами классов М и G. При обследовании новорожденных в этом случае также исключаются ложноположительные результаты анализа, связанные с выявлением IgM, направленных против материнских антитрепонемных IgG.
В качестве вариантов ИФА за рубежом нашли широкое применение enzyme immune assay (EIA) и система ICE Syphilis. В последней в ячейках планшета сорбирована смесь антител к IgM и IgG, а также трех рекомбинантных белков T. pallidum. Положительные результаты тестируются в этой же тест-системе в двух повторах для выдачи окончательного результата.
В России был разработан ряд тест-систем для серодиагностики сифилиса методом ИФА с отечественными реагентами. Эти системы обладают высокой специфичностью и чувствительностью.
Помимо вышеперечисленных, существуют также другие варианты ИФА, в том числе допускающие прямое выявление возбудителя в крови (прямой ИФА), дот-ИФА с постановкой реакции на полосках нитроцеллюлозы, ИФА с капиллярной кровью, а также иммуноблоттинг, или Western Blot, с одновременным выявлением АТ к различным компонентам возбудителя.
Современной улучшенной модификацией ИФА является иммуноблоттинг.
ИХА (иммунохемилюминесцентный анализ), ИХЛ (иммунохемилюминесценция)
С развитием лабораторной диагностики в условиях модернизации здравоохранения РФ в практику лабораторий вошла автоматизация лабораторных исследований, которая позволяет стандартизовать аналитические этапы исследований. Это способствует повышению качества диагностики. С внедрением автоматизации стали применяться новые высокотехнологичные методы, обладающие высокой чувствительностью и специфичностью, такие как иммунохемилюминесцентный анализ (ИХА) (chemiluminescence immunoassay — CLIA)
Хемилюминесценция — процесс излучения фотонов при переходе электронно-возбужденных продуктов окислительных химических реакций в исходное энергетическое состояние. В ходе реакции хемилюминесценции выделяется значительное количество энергии, и квантовый выход излучаемого света достаточно высок. Из всех неизотопных методов хемилюминесценция обеспечивает наиболее высокую чувствительность. Для иммунометрических методов чувствительность хемилюминесценции на порядки превосходит чувствительность радиоиммуноанализа.
Метод иммунохемилюминесценции (ИХЛ) в настоящее время нашел свое применение при диагностике маркеров опухолей, аутоиммунных заболеваний, диабета, кардиомаркеров, гормонов (щитовидной железы, надпочечников, женских и мужских половых гормонов), torch-инфекций, вирусных гепатитов, вирусов группы герпеса.
На основе метода иммунохемилюминесценции разработан ряд высокочувствительных и специфичных (98—100%) тест-систем для диагностики сифилиса, применяемых в основном за рубежом.
В методе в качестве антигенов используются полученные генно-инженерными методами рекомбинантные липопротеины, которые являются полными аналогами антигенов T.pallidum.
Метод ИХА по результатам клинического исследования получил признание и рекомендован к применению в лабораторной диагностике сифилиса в Российской Федерации в качестве скринингового и подтверждающего теста при наличии в лабораториях соответствующего оборудования. В 2012 г. ИХА был включен в качестве скринингового и подтверждающего теста для диагностики сифилиса в Клинические рекомендации по ведению больных с инфекциями, передаваемыми половым путем, и урогенитальными инфекциями
Таким образом, использование высокотехнологичного ИХА, вошедшего в практику как мировой, так и отечественной лабораторной диагностики с внедрением автоматизации, обеспечивает следующие преимущества:
- исключение влияния субъективных факторов на аналитическом этапе исследования
- безопасность персонала при выполнении исследований потенциально инфицированного биологического материала
- повышение скорости получения результатов пациентом
- стандартизацию исследований и контроль качества исследования
- выдачу надежных достоверных результатов пациентам
- высокое качество клинических лабораторных исследований.
По чувствительности метод ИХА сопоставим с методом радиоиммунного анализа, а по простоте исполнения, безопасности для персонала и многим другим параметрам – превосходит его.
Метод ИХА, обладающий высокой чувствительностью и специфичностью (98–100%), дает возможность количественного определения уровня антител к возбудителю сифилиса, может быть использован для подтверждения сифилитической инфекции и скрининга. Ограничения применения: не может быть использован для контроля эффективности терапии, может давать ложноположительный результат.
Иммунохроматография (ИХГ).
Относительно новыми для использования в Российской Федерации являются методы выявления трепонемоспецифических антител, основанные на методах иммунохроматографии (ИХГ). Как и в методе ИХА, в качестве антигенов используются рекомбинантные липопротеины, полученные генно-инженерными методами (например: антигены Tp15, Tp17, Tp47) и биосинтетический пептид TmрА. Перечисленные антигены также используются в разных сочетаниях в составе иммуносорбентов в ИФА и иммуноблоттинге.
Метод ИХГ позволяет быстро определять содержание трепонемоспецифических антител к возбудителю сифилиса в образцах сыворотки и цельной крови без использования специального лабораторного оборудования и применяется при оказании первичной медико-санитарной помощи, в том числе по эпидемиологическим показаниям.
Ограничения применения: не может быть использован для контроля эффективности терапии,может давать ложноположительный результат.
ПБТ (простые быстрые тесты у постели больного)
Относительно недавно в серодиагностике сифилиса начало развиваться направление по разработке так называемых простых быстрых тестов (ПБТ), или тестов у постели больного (Point-of-care — РОС). Простые быстрые тесты у постели больного, или иммунохроматографические тесты позволяют проводить быстрое определение содержания трепонемоспецифических антител к возбудителю сифилиса в образцах сыворотки и цельной крови без использования специального лабораторного оборудования и применяться при оказании первичной медико-санитарной помощи, в том числе по эпидемиологическим показаниям. Ограничения применения: не могут быть использованы для контроля эффективности терапии, могут давать ложноположительный результат.
Эти тесты основаны на иммунохроматографическом определении антител к трепонемным антигенам бледной трепонемы я выполняются на стрипах; при этом можно использовать как цельную кровь, так и сыворотку (Herring A., Ballard R. et al, 2006). Формат тестов позволяет проводить исследования при отсутствии специального оборудования и без использования электричества. Однако ввиду относительно невысокой чувствительности и специфичности эти тесты пока не находят своего широкого применения в практике.
Иммуноблотинг (Western Blot)
В последние годы появились методы исследования, направленные на обнаружение и анализ содержания антител к каждому антигену бледной трепонемы раздельно. Один из таких методов — это метод иммунного блота (или блоттинга, имммуноблотинга, Western blot), который применяют для определения IgG- либо IgM-антител к бледной трепонеме. Метод иммуноблоттинга является модификацией иммуноферментного анализа — вариантом ИФА.
Имммуноблотинг является одним из самых современных методов серодиагностики сифилиса и активно используется за рубежом. Свое название ("западный блоттинг") он получил в качестве юмористического ответа на названия техник определения ДНК ("южный блоттинг") и РНК ("северный блоттинг").
1. История метода
Иммуноблоттинг (Western blot) используют для определения IgG- либо IgM-антител к антигенам бледной трепонемы (Herremans М. et al., 2007).
2. Классический иммуноблот
Классический иммуноблот (Western Blot Analysis) сочетает в себе иммуноферментный анализ и применение электрофоретического метода. Белки-антигены возбудителя сифилиса предварительно разделяют методом электрофореза и переносят на носитель — нитроцеллюлозную мембрану (стрип). Этот перенос и называется блоттингом. Затем этот носитель с разделенными точками (blots), обрабатывают исследуемой сывороткой и антителами к IgG или IgM, меченными ферментами либо радиоактивными веществами. Метод предполагает использование природных или рекомбинантных белков трепонемы.

Электрофорез - это разделение заряженных соединений на основе их подвижности в электрофоретическом поле. При наложении разности потенциалов в какой-то среде положительно заряженные молекулы движутся к отрицательно заряженному электроду, а отрицательно заряженные - к положительному электроду.
Большинство глобулярных белков собраны таким образом, что большая часть заряженных групп, а именно гидрофильных, расположена на поверхности белка, тогда как незаряженные, гидрофобные остатки погружены во внутрь глобулы. В электрическом поле в соответствии со своим зарядом белки мигрируют по направлению к противоположно заряженному электроду.
Электрофоретическое разделение белков производят в синтетический гелевой среде на основе полиакриламида. Для разделения белков в соответствии с их молекулярной массой перед началом электрофореза белковую смесь преинкубируют в присутствии додецилсульфата натрия (ДСН).
Детальные исследования зарубежных ученых Weber и Osborn (1969) показали, что после такой обработки единственным фактором, который может повлиять на подвижность белков в полиакриламидном геле (ПААГ) является размер белка, а точнее его молекулярная масса. Это позволило применить метод электрофореза в ПААГ в присутствии ДСН для достаточно точного определения молекулярной массы белков и пептидов. В зарубежной литературе этот метод был назван SDS-PAGE (sodium dodecyl sulphate-polyacrylamide gel electrophoresis).
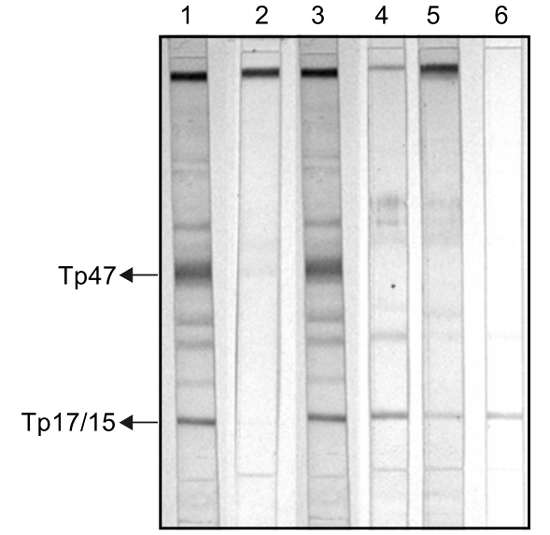 Профиль реактивности в классическом WB-тесте с природными антигенами (метод электрофореза в полиакриламидном геле с додецилсульфатом натрия). (1) - контрольный положительный результат, (2) - контрольный отрицательный результат, (3-6) - клинические образцы.
Профиль реактивности в классическом WB-тесте с природными антигенами (метод электрофореза в полиакриламидном геле с додецилсульфатом натрия). (1) - контрольный положительный результат, (2) - контрольный отрицательный результат, (3-6) - клинические образцы.В тестах на сифилис с помощью данного метода, предварительно очищенная и разрушенная до составных компонентов бледная трепонема подвергается электрофорезу в полиакриламидном или агарозном геле. При этом входящие в ее состав антигены разделяются по молекулярной массе.
Затем методом вертикального электрофореза антигены переносят на полоску нитроцеллюлозы, которая отныне содержит невидимый глазом спектр антигенных полос, характерный для бледной трепонемы.
При проведении анализа на нитроцеллюлозную полоску (стрип) наносится исследуемый материал (сыворотка, плазма крови пациента и др.). Если в пробе есть специфические антитела, то в процессе инкубации они прочно связываются со строго соответствующими (комплементарными) им антигенными полосами и образуют комплекс “антиген – антитело”.
После удаления несвязавшихся иммуноглобулинов во время отмывания стрипа следует инкубация с конъюгатом – меченными ферментом антителами к иммуноглобулинам человека (антитела к IgG или IgM человека), в ходе которой на поверхности мембраны происходит присоединение к имеющимся комплексам “антиген – антитело” антител, меченных ферментом.
После удаления несвязавшегося конъюгата в ходе инкубации с раствором субстрата происходит взаимодействие фермента с субстратом, в результате чего развивается цветная реакция – окрашивание участков мембраны (в виде полос), где располагаются отдельные антигены бледной трепонемы, антитела к которым находились в исследуемой сыворотке. Интенсивность окрашивания зависит от количества связавшихся антител из сыворотки. Результат реакции оценивается визуально.
Наличие полос на определенных участках нитроцеллюлозной пластины подтверждает присутствие в исследованной сыворотке антител к строго определенным антигенам бледной трепонемы.
Определяемые с помощью этого метода иммунодетерминанты 15, 5, 17, 44,5, 47 кД обладают диагностической значимостью при сифилисе. Ig G-иммуноблоттинг по чувствительности и специфичности подобен РИФ с абсорбцией (РИФ abs). Ig М-иммуноблоттинг может служить диагностическим тестом для врожденного сифилиса.
3. Иммуноблот в формате линейного иммунного анализа
Линейный иммунологический анализ (line immunoassay, LIA) позволяет одновременно определять антитела к антигенам бледной трепонемы в сыворотке или плазме крови человека. Антигены заранее нанесены на тест-полоски (стрипы), которые поставляются в составе коммерческих диагностических наборов.
Стрипы изготавливаются из нитроцеллюлозной мембраны, полиамидной с пластиковой подложкой или нейлоновой мембраны с пластиковой основой. При изготовлении, на тест-полоску помещают несколько дискретных антигенов в виде отдельных антигенных линий. Помимо этих антигенов сифилиса, на каждую полосу наносятся еще четыре контрольных линии: стрептавидин и контрольные пробы (3 + , 1 + и ± линия среза).
Для полосок используются искусственные антигены, полученные генно-инженерными способами — рекомбинантные белки или синтетические полипептидные конструкции. Это аналоги поверхностных антигенов бледной трепонемы — TpN15, TpN17, TpN47 и TmpA с молекулярной массой 15, 17, 47 kDа и 44,5 (ТmpА), где kDа=kiloDaltons. С их помощью определяют сывороточные антитела к различным иммунодоминантным компонентам возбудителя.
Инкубация испытательного образца проходит в кювете, куда также помещается индикаторная полоса. Антитела к T. рallidum определяются по связыванию с антигенами, нанесенными на тест-полоски. Если в образце имеются специфичные для T. pallidum антитела, они образуют связи с отдельными линиями антигенов. При взаимодействии антител, содержащихся в испытуемой сыворотке, с дискретными антигенами Т. pallidum, помещенными тест-полоску, образуется комплекс антиген-антитело в виде визуально определяемых цветных полос.
При учете результатов иммуноблотинга оценивают реактивность сыворотки к каждому из антигенов в отдельности. Суммарный положительный ответ выдается при получении результата одновременно с двумя или тремя из представленных антигенов.
Исследовательские процедуры проводятся вручную или на специальном анализаторе, с интерпретацией результатов с помощью специализированной компьютерной программы для инфекционных заболеваний.
За счет высокой степени очистки рекомбинантных антигенов и одновременного выявления антител к наиболее иммуногенным детерминантам возбудителя сифилиса, метод обладает высокой чувствительностью и специфичностью.
.
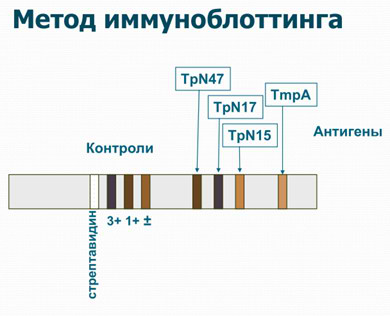
4. Учет результатов
Для считывания интенсивности окрашивания антигенных полос на стрипах разработаны фотометры, работа которых основана на отражении сигнала, что исключает субъективную оценку и дает потенциальную возможность автоматизации.
5. При каких периодах заболевания лучше использовать
Тесты, использующие метод иммуноблоттинга, могут определять специфические антитела к антигенам бледной трепонемы на очень ранней стадии заболевания. Наиболее значимыми в диагностике сифилиса являются антитела к антигенам бледной трепонемы TpN15, TpN17, TmpA и TpN47. Эти антигены — мембранные белки, имеющие молекулярную массу 15, 17, 44,5 и 47 кДа соответственно.
При внедрении в организм человека бледной трепонемы, противосифилитические антитела появляются в таком порядке: сначала развивается иммунный ответ к антигенам TpN17, затем к TpN47, после TpN15 и позже всех TmpA. При учете результатов теста оценивают реактивность сыворотки к каждому из них в отдельности. Например, когда в линейном блоте имеется реактивность только к антигенной линии TpN17 и TpN47, это означает, что болезнь в начальной стадии. Чем больше антигенных линий становятся реактивными, тем дальше развивается инфекция. При лечении сифилиса картина реактивности в этом тесте меняется.
Определение IgM к протеинам с молекулярной массой 15,17, 41, 47 кДа позволяют выявить 29,2% больных при вторичном сифилисе, 12,5% – при раннем скрытом сифилисе и 8,0% – при серорезистентности. Поиск IgG к тем же молекулам характеризуется чувствительностью 61,6% при серорезистентности и 100% при вторичном и раннем скрытом сифилисе.
6. Чувствительность и специфичность
Согласно данным литературы, чувствительность и специфичность теста очень высокие — 99,6—100 и 99,3—99,5 % соответственно. В классическом методе это достигается за счет электрофоретического разделения белков, глико- и липопротеинов и максимальной специфичности детектирующих иммунных сывороток или моноклональных антител. В оптимально отработанных условиях с помощью иммуноблоттинга можно обнаруживать антиген в количествах менее 1 нг в испытуемом объеме.
Чувствительность линейного блота также составляет 99.6%, а специфичность находится в диапазоне между 99.3% и 99.5%.
По оценке специалистов иммуноблоттинг с рекомбинантными высокоспецифичными антигенами по чувствительности и специфичности аналогичен РИФ-абс.
Согласно данным зарубежной литературы и результатам изучения в ЦНИКВИ, метод иммуноблоттинга обладает при диагностике сифилиса высокой чувствительностью (98,8-100%) и специфичностью (97,1-100%).
7. Область применения метода
Иммуноблотинг (иммуноблот) является высокоспецифичным и высокочувствительным референтным методом. Высокие чувствительность и специфичность позволяют рассматривать этот метод как подтверждающий тест на сифилис. Метод может применяться для подтверждения диагноза, а также в случае, если другие трепонемные тесты дают сомнительные и противоречивые результаты. С помощью иммуноблоттинга можно подтвердить диагноз у пациентов с положительными или неопределенными результатами анализов, полученных в том числе и при помощи РПГА или ИФА.
8. Источники и причины ошибок при постановке, ложноположительные и ложноотрицательные результаты
Ложноположительные результаты очень редки. Ложноотрицательные результаты бывают также достаточно редко и наблюдаются у больных с иммунодефицитами – чаще у ВИЧ- инфицированных и при эффекте диагностического «окна» из-за задержки синтеза антител, а также при ошибках на этапе постановки.
Использование современных тест-систем диктует точное соблюдение всех требований, предъявляемых как к материалу, так и к выполнению постановки реакции. В основном, источник ошибок — нарушение порядка и технологии проведения исследования (особенно для классического вестерн-блота), несоблюдение рекомендаций производителей тест-наборов. . Ошибки могут быть также допущены при сборе, доставке, хранении проб сыворотки крови, а также при выполнении тестов. Помимо испорченных образцов, среди других возможных причин - использование тест-наборов с истекшим сроком годности, а также ошибки при анализе результатов исследования.
9. Особенности, преимущества и недостатки
Уникальность иммуноблота заключается в его высокой информативности и достоверности результатов.
Тест не требует высокоочищенных антигенов, референтных и контрольных сывороток. Идентификация мишени антител основана на молекулярном весе белка, с которым реагируют антитела из сыворотки пациента. В одной реакции может быть обнаружено связывание антител с несколькими антигенами, каждый из которых может быть точно охарактеризован. За счет этого иммуноблоттинг обладает рядом преимуществ перед другими методами выявления антител, результаты которых зависят от стандартизации, чувствительности, качества субстрата, нестабильности или нерастворимости определенных антигенов
Метод легко воспроизводим, относительно прост в исполнении и интерпретации результатов, дает возможность определять спектр антител сразу к нескольким антигенам Т. pallidum и оценивать вклад в общую реакцию антител различной специфичности.
Применение высокоочищенных рекомбинантных и пептидных антигенов снижает до минимума неспецифическую реактивность сывороток. Использование метода дает возможность отказа от трудоемких и субъективных методов, представляющих опасность для исследователя (перевивка штаммов Г. pallidum, работа с патогенной Т. pallidum при постановке реакции). Это определяет предпочтение метода иммуноблоттинга перед другими трепонемными тестами (РИФ и в особенности РИБТ) для диагностики сифилиса.
10. Модификации метода
Существует несколько коммерческих тест-систем на основе данного метода. Одни из них выполнены в формате вестерн-блота, состоят из стрипов, на которые перенесены белковые компоненты T. pallidum, предварительно разделенные электрофорезом в полиакриламидном геле.
Другие выполнены в формате линейного блота, состоят из стрипов, на которых в виде дискретных линий сорбированы рекомбинантные и синтетические полипептиды — аналоги поверхностных антигенов T. pallidum, TpN15, TpN17, TpN47 и TmpA.
Результаты вестерн-блота труднее интерпретировать, так как на стрипах выявляется большое разнообразие антител, многие из которых являются группоспецифическими. Напротив, интерпретация результатов линейного блота не вызывает затруднений; кроме того, дополнительные контрольные линии, нанесенные на стрип, позволяют проводить полуколичественную оценку уровня антител к четырем антигенам T. pallidum.
xMAP-технология
хМАР — современная технология, позволяющая проводить многопараметрические исследования путем одновременной детекции множества аналитов в одном биологическом образце. В качестве твердой фазы используются окрашенные микросферы, покрытые захватывающими реагентами (олигонуклеотидами, антителами, антигенами).
Исследуемый образец добавляется к раствору, в котором содержатся микросферы. Выявляемые в образце аналиты связываются с соответствующей микросферой, после чего в раствор вносится детектирующий агент (детектирующие антитела, флюоресцентная метка). Для детекции определяемого аналита используется система двух лазеров, позволяющих проводить как качественную оценку наличия аналита в пробе (для этого используется красный лазер, классифицирующий микросферы по цвету), так и количественную оценку содержания аналита в пробе (для этого используется зеленый лазер).
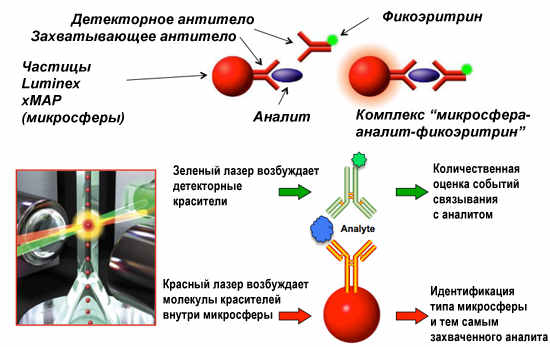
Исследование осуществляется в автоматическом режиме на анализаторах типа Bio-Plex 200 (bio-rad), Bio-Plex2200 (bio-rad), Luminex100 (luminex), Luminex200 (luminex) снабженных программным обеспечением.
Ппроизводительность xMAP-технологии значительно превышает показатели классического твердофазного иммуноферментного анализа (ИФА) при существенно меньшем объеме биоматериала.
хМАР-технология, обладающая высокой аналитической чувствительностью, в настоящее время используется для решения широкого круга клинических задач. С ее помощью в одном образце биологического материала осуществляется одновременная детекция известных онкомаркеров, кардиомаркеров, маркеров острой фазы и сахарного диабета, широкого спектра цитокинов, хемокинов, факторов роста. Одномоментное выявление множества аналитов в одном биологическом образце позволяет существенно сократить время обследования пациента. К настоящему времени разработан ряд тест-систем для выявления антител к возбудителям ИППП, в частности сифилитической инфекции, методом хМАР.
запись по телефону 8 (985) 970-30-92 ежедневно с 7.00 до 23.00
ПРИЕМ ТОЛЬКО ПО ЗАПИСИ! ЗВОНИТЕ.
Медицинский центр "На Ленинском" - ежедневно. ЗАПИСЬ!
Медицинский центр "На Самотечной" - cуббота, воскресенье.
По предварительной записи!



