Что такое антигены и антитела. Реакция антиген-антитело.
Что такое антигены
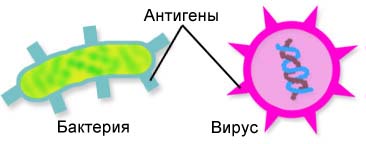
Антигены - это любые вещества, содержащиеся в микроорганизмах и других клетках (или выделяемые ими), которые несут в себе признаки генетически чужеродной информации и которые потенциально могут быть распознаны иммунной системой организма. При введении во внутреннюю среду организма эти генетически чужеродные вещества способны вызывать иммунный ответ различных типов.
Каждый микроорганизм, как бы примитивно он ни был устроен, содержит несколько антигенов. Чем сложнее его структура, тем больше антигенов можно обнаружить в его составе.
Антигенными свойствами обладают различные элементы микроорганизма — жгутики, капсула, клеточная стенка, цитоплазматическая мембрана, рибосомы и другие компоненты цитоплазмы, а также различные продукты белковой природы, выделяемые бактериями во внешнюю среду, в том числе токсины и ферменты.
Различают экзогенные антигены (поступающие в организм извне) и эндогенные антигены (аутоантигены — продукты собственных клеток организма), а также антигены, вызывающие аллергические реакции, — аллергены.
Что такое антитела
 Организм непрерывно встречается с разнообразными антигенами. Он подвергается атаке как извне — со стороны вирусов и бактерий, так и изнутри — со стороны клеток организма, приобретающих антигенные свойства.
Организм непрерывно встречается с разнообразными антигенами. Он подвергается атаке как извне — со стороны вирусов и бактерий, так и изнутри — со стороны клеток организма, приобретающих антигенные свойства.
Антитела – белки сыворотки крови, которые вырабатываются плазматическими клетками в ответ на проникновение антигена в организм. Антитела вырабатываются клетками лимфоидных органов, и циркулируют в плазме крови, лимфе и других жидкостях организма.
Главная важная роль антител — это распознавание и связывание чужеродного материала (антигена), а также запуск механизма уничтожения этого чужеродного материала. Существенным и уникальным свойством антител служит их способность связывать антиген непосредственно в том виде, в каком он проникает в организм.
Антитела обладают способностью отличать один антиген от другого. Они способны к специфическому взаимодействию с антигеном, но взаимодействуют только с тем антигеном (за редким исключением), который индуцировал их образование и подходит к ним по пространственной структуре. Эта способность антитела получила название комплементарности.
Полного понимания молекулярного механизма образования антител пока не существует. Не изучены молекулярные и генетические механизмы, лежащие в основе распознавания миллионов различных антигенов, встречающихся в окружающей среде.
Антитела и иммуноглобулины
.
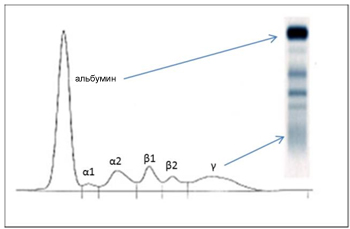 В конце 30-х годов XX века началось изучение молекулярной природы антител. Одним из способов исследования молекул являлся электрофорез, который был введен в практику в эти же годы. Электрофорез позволяет разделить белки по их электрическому заряду и молекулярной массе. При электрофорезе белков сыворотки обычно получается 5 основных полос, которые соответствуют (от + к -) фракциям альбумина, альфа1-, альфа2-, бета- и гамма-глобулинов.
В конце 30-х годов XX века началось изучение молекулярной природы антител. Одним из способов исследования молекул являлся электрофорез, который был введен в практику в эти же годы. Электрофорез позволяет разделить белки по их электрическому заряду и молекулярной массе. При электрофорезе белков сыворотки обычно получается 5 основных полос, которые соответствуют (от + к -) фракциям альбумина, альфа1-, альфа2-, бета- и гамма-глобулинов. В 1939 году шведский химик Арне Тиселиус и американский иммунохимик Элвин Кэбет (Tiselius, Kabat) использовали электрофорез, чтобы разделить на фракции сыворотку крови иммунизированных животных. Ученые показали, что антитела содержатся в определённой фракции белков сыворотки. А именно — антитела относятся, в основном, к гамма-глобулинам. Так как часть попадала также в область бета-глобулинов, то для антител был предложен лучший термин — иммуноглобулины.
В соответствии с международной классификацией, совокупность сывороточных белков, обладающих свойствами антител, называют иммуноглобулинами и обозначают символом Ig (от слова «Immunoglobulin»).
Термин «иммуноглобулины» отражает химическую структуру молекул этих белков. Термин «антитело» определяет функциональные свойства молекулы и учитывает способность антитела реагировать только с определенным антигеном.
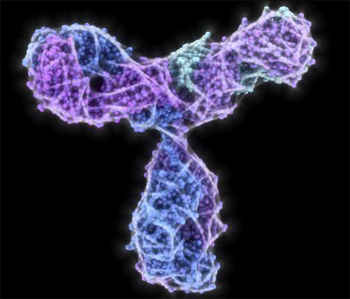
Раньше предполагалось, что иммуноглобулины и антитела – синонимы. В настоящее время существует мнение, что все антитела являются иммуноглобулинами, но не все иммуноглобулиновые молекулы обладают функцией антител.
Мы говорим об антителах только относительно антигена, т.е. если антиген известен. Если мы не знаем антиген, комплементарный некоему иммуноглобулину, который оказался у нас «в руках», то мы имеем только иммуноглобулин. В любой антисыворотке, кроме антител против данного антигена, имеется большое количество иммуноглобулинов, антительную активность которых не удалось обнаружить, однако это не означает, что данные иммуноглобулины не являются антителами к каким-либо другим антигенам. Вопрос о существовании молекул иммуноглобулинов, изначально не обладающих свойствами антител, пока остается открытым.
Антитела (АТ, иммуноглобулины, ИГ, Ig) являются центральной фигурой гуморального иммунитета. Основную роль в иммунной защите организма играют лимфоциты, которые подразделяются на две основные категории – Т-лимфоциты и В-лимфоциты.
Антитела или иммуноглобулины (Ig) синтезируются В-лимфоцитами, а точнее антителообразующими клетками (АОК). Синтез антител начинается в ответ на попадание во внутреннюю среду организма антигенов. Для синтеза антител B-клеткам необходим контакт с антигеном и вызванное им созревание B-клеток в антителообразующие клетки. Значительное число антител вырабатывают образовавшиеся из В-лимфоцитов так называемые плазматические клетки — АОК, выявляемые в крови и тканях. Иммуноглобулины содержатся в большом количестве в сыворотке, в межклеточной жидкости и других секретах, обеспечивая гуморальный ответ.
Классы иммуноглобулинов
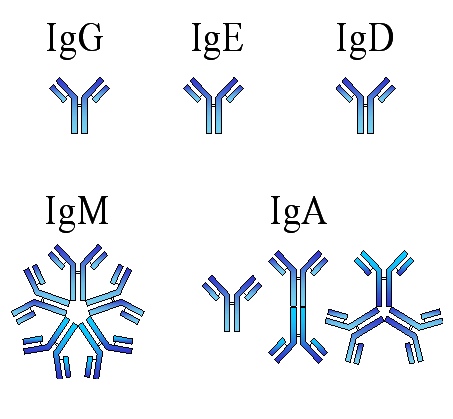
Иммуноглобулины (Ig) различаются по структуре и по выполняемым функциям. У человека обнаружены 5 различных классов иммуноглобулинов: IgG, IgA, IgM, IgE, IgD, часть из которых ещё подразделяется на подклассы. Подклассы есть у иммуноглобулинов классов G (Gl, G2, G3, G4), А (А1, А2) и M (M1, M2).
Классы и подклассы, вместе взятые, называют изотипами иммуноглобулинов.
Антитела разных классов различаются по размерам молекул, заряду белковой молекулы, аминокислотному составу и содержанию углеводного компонента. Наиболее изученным классом антител является IgG.
В сыворотке крови человека в норме преобладают иммуноглобулины класса IgG. Они составляют приблизительно 70–80% от общего количества сывороточных антител. Содержание IgA - 10-15%, IgM - 5-10%. Содержание иммуноглобулинов класса IgE и IgD очень мало - около 0.1% для каждого из этих классов.
Не следует думать, что антитела против того или иного антигена принадлежат только к какому-то одному из пяти классов иммуноглобулинов. Наоборот, антитела против одного и того же антигена могут быть представлены разными классами Ig.
Важнейшую диагностическую роль играет определение антител классов М и G, так как после инфицирования человека первыми появляются антитела класса М, затем класса G, и последними иммуноглобулины А и Е.
Иммуногенность и антигенность антигенов
В ответ на попадание антигенов в организм начинается целый комплекс реакций, направленный на освобождение внутренней среды организма от продуктов чужеродной генетической информации. Такая совокупность защитных реакций иммунной системы называется иммунным ответом.
Иммуногенностью называется способность антигена вызывать иммунный ответ, то есть индуцировать специфическую защитную реакцию иммунной системы. Иммуногенность также можно описать, как способность создавать иммунитет.
Иммуногенность в значительной степени зависит от природы антигена, его свойств (молекулярного веса, подвижности молекул антигена, формы, структуры, способности к изменению), от пути и режима попадания антигена в организм, а также дополнительных воздействий и генотипа реципиента.
Как упомянуто выше, одной из форм реагирования иммунной системы в ответ на внедрение в организм антигена является биосинтез антител. Антитела способны связывать антиген, вызвавший их образование, и тем самым защищать организм от возможного вредного действия чужеродных антигенов. В связи с этим, вводится понятие антигенности.
Антигенность – это способность антигена специфически взаимодействовать с факторами иммунитета, а именно вступать во взаимодействие с продуктами вызванного именно этим веществом иммунного ответа (антителами и Т- и В-антиген-распознающими рецепторами).
Некоторый термины молекулярной биологии
Липиды (от др.-греч. λίπος — жир) — обширная группа довольно разнообразных природных органических соединений, включающая жиры и жироподобные вещества. Липиды содержатся во всех живых клетках и являются одним из основных компонентов биологических мембран. Они нерастворимы в воде и хорошо растворимы в органических растворителях. Фосфолипиды — сложные липиды, содержащие в себе высшие жирные кислоты и остаток фосфорной кислоты.
Конформация молекул (от лат. conformatio — форма, построение, расположение) — геометрические формы, которые могут принимать молекулы органических соединений при вращении атомов или групп атомов (заместителей) вокруг простых связей при сохранении неизменными порядка химической связи атомов (химического строения), длины связей и валентных углов.
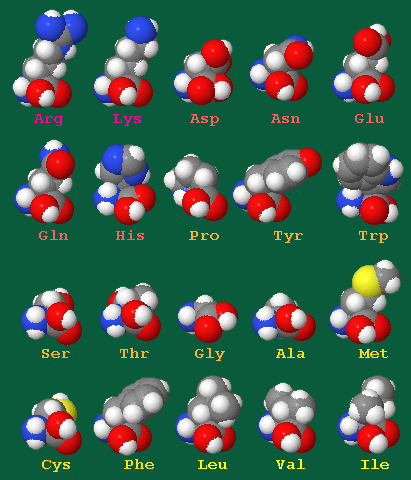
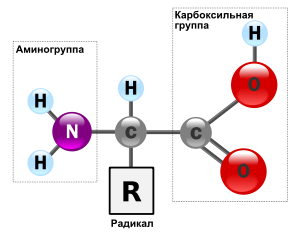
Аминокислоты — органические соединения (кислоты) особой структуры. В их молекулах одновременно содержатся аминогруппы (NH2) и карбоксильные группы (СООН). Все аминокислоты состоят всегоиз 5 химических элементов: С, H, O, N, S.
Пептиды (греч. πεπτος — питательный) — семейство веществ, молекулы которых построены из двух и более остатков аминокислот, соединённых в цепь пептидными (амидными) связями. Пептиды, последовательность которых длиннее примерно 10-20 аминокислотных остатков, называются полипептидами.
В полипептидной цепи различают N-конец, образованный свободной α-аминогруппой и С-конец, имеющий свободную α-карбоксильную группу. Пептиды пишутся и читаются с N-конца к С-концу— с N-концевой аминокислоты к С-концевой аминокислоте.
Аминокислотные остатки — это мономеры аминокислот, входящих в состав пептидов. Аминокислотный остаток, имеющий свободную аминогруппу, называется N-концевым и пишется слева, а имеющий свободную α-карбоксильную группу - С-концевым и пишется справа.
Белками обычно называют полипептиды, содержащие примерно от 50 аминокислотных остатков. В качестве синонима термина «белки» также используется термин «протеины» (от греч. protos - первый, важнейший). Молекула любого белка имеет четко определенную, достаточно сложную, трехмерную структуру.
Аминокислотные остатки в белках принято обозначать с помощью трёх-буквенного или одно-буквенного кода. Трёх-буквенный код представляет собой аббревиатуру от английских названий аминокислот и часто используется в научной литературе. Одно-буквенный код по большей части не имеет интуитивно понятной связи с названиями аминокислот и используется в биоинформатике для представления последовательности аминокислот в виде текста, удобного для компьютерного анализа.
Пептидный остов. В полипептидной цепи многократно повторяется последовательность атомов -NH-CH-CО- .Эта последовательность и формирует пептидный остов. Полипептидная цепь состоит из полипептидного остова (скелета), имеющего регулярную, повторяющуюся структуру, и отдельных боковых групп (R-групп).
Пептидные связи соединяют аминокислоты в пептиды. Пептидные связи образуются при взаимодействии α-карбоксильной группы одной аминокислоты и α-аминогруппы от последующей аминокислоты. Пептидные связи очень прочны и самопроизвольно не разрываются при нормальных условиях, существующих в клетках.
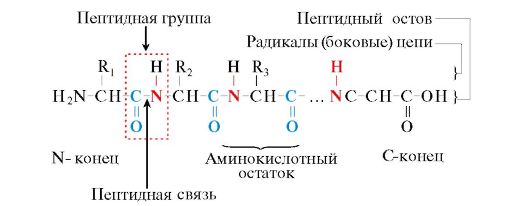
Многократно повторяющиеся в молекулах пептидов группы атомов —СО—NH— называются пептидными группами. Пептидная группа обладает жесткой планарной (плоской) структурой.
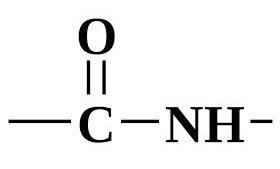
Конформация белков — расположение полипептидной цепи в пространстве. Пространственная структура, характерная для молекулы белка, образуется за счет внутримолекулярных взаимодействий. Линейные полипептидные цепи индивидуальных белков за счёт взаимодействия функциональных групп аминокислот приобретают определённую трёхмерную структуру, которая и называется «конформацией белков».
Процесс формирования функционально активной конформации белка носит название фолдинг. Жёсткость пептидной связи уменьшает количество степеней свободы полипептидной цепи, что играет большую роль в процессе фолдинга.
Глобулярные и фибриллярные белки. Изученные к настоящему времени белки можно разделить на два больших класса по способности принимать в растворе определенную геометрическую форму: фибриллярные (вытянyтые в нить) и глобулярные (свернутые в клубок). Полипептидные цепи фибриллярных белков вытянуты, расположены параллельно друг другу и образуют длинные нити или слои. В глобулярных белках полипептидные цепи плотно свернyты в глобулы — компактные структуры сферической формы.
Следует отметить условность деления белков на фибриллярные и глобулярные, так как существует большое число белков с промежуточной структурой.
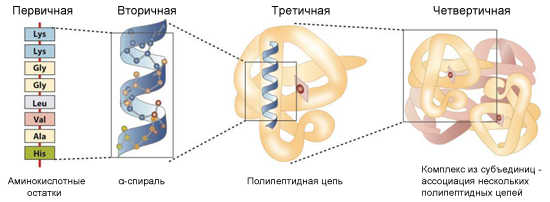
Первичная структура белка (primary structure of protein) — это линейная последовательность аминокислот, составляющих белок, в полипептидной цепи. Аминокислоты соединены между собой пептидными связями. Последовательность аминокислот записывают, начиная от С-конца молекулы, в направлении к N-концу полипептидной цепочки.
П.с.б — это простейший уровень структурной организации белковой молекулы. Первая П.с.б. была установлена Ф. Сенгером для инсулина (Нобелевская премия за 1958 г.).
Вторичная структура белка (secondary structure of protein)— укладка полипептидной цепи белка в результате взаимодействия между близкорасположенными аминокислотами в составе одной и той же пептидной цепочки — между аминокислотами расположенными через считанные остатки друг от друга.
Вторичная структура белков - это пространственная структура, которая образуется в результате взаимодействий между функциональными группами, входящими в состав пептидного остова.
Вторичная структура белков обусловлена способностью групп пептидной связи к водородным взаимодействиям—между функциональными группами -С=О и - NH- пептидного остова. При этом пептид стремится принять конформацию с образованием максимального числа водородных связей. Однако возможность их образования ограничивается характером пептидной связи. Поэтому пептидная цепь приобретает не произвольную, а строго определенную конформацию.
Вторичная структура образуется из сегментов полипептидной цепи, которые участвуют в формировании регулярной сетки водородных связей.
Другими словами, под вторичной структурой полипептида понимают конформацию его основной цепи (остова) без учета конформации боковых групп.
Полипептидная цепь белка, складываясь под действием водородных связей в компактную форму, может образовывать некоторое количество регулярных структур. Таких структур известно несколько: α (альфа)-спираль , β (бета)-структура (другое название — β-складчатый слой или β-складчатый лист), беспорядочный клубок и поворот. Редким видом вторичной структуры белков являются π-спирали. Первоначально исследователи считали, что данный вид спирали в природе не встречается, однако позже эти спирали были открыты в белках.
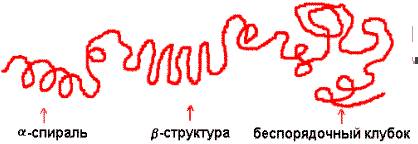
α -спираль и β-структура являются энергетически наиболее выгодными конформациями, поскольку обе они стабилизированы водородными связями. Кроме того, и α-спираль, и β-структура дополнительно стабилизируются благодаря плотной упаковке атомов основной цепи, которые подогнаны друг к другу, как кусочки одной картинки-головоломки.
Эти фрагменты и их сочетание в некотором белке, если они имеются, также принято называть вторичной структурой этого белка.
В структуре глобулярных белков могут встречаться фрагменты регулярного строения всех типов в любой комбинации, но может не быть и ни одного. В фибриллярных белках все остатки принадлежат какому-то одному типу: например, шерсть содержит α-спирали, а шелк — β-структуры.
Таким образом, чаще всего вторичная структура белка — это укладка полипептидной цепи белка в α-спиральные участки и β-структурные образования (слои) с участием водородных связей. Если водородные связи образуются между участками изгиба одной цепи, то их называют внутрицепочечными, если между цепями – межцепочечные. Водородные связи располагаются перпендикулярно полипептидной цепи.
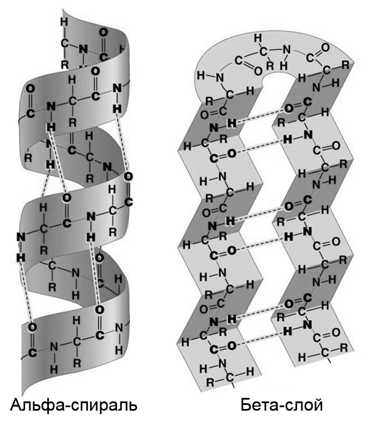
α-спираль—образуется внутрицепочечными водородными связями между NH группой одного остатка аминокислоты и CO-группой четвертого от нее остатка. Средняя длина α-спиралей в белках - 10 аминокислотных остатков
В α-спирали водородные связи образуются между атомом кислорода карбонильной группы и водородом амидного азота 4-й от него аминокислоты. В образовании этих водородных связей вовлечены все группы C=O и N-H основной полипептидной цепи. Боковые цепи аминокислотных остатков располагаются по периферии спирали и не участвуют в образовании вторичной структуры.
β-структуры формируются между линейными областями пептидного остова одной полипептидной цепи, образуя при этом складчатые структуры (несколько зигзагообразных полипептидных цепей).
β-структура формируется за счет образования множества водородных связей между атомами пептидных групп линейных цепей. В β-структурах водородные связи образуются между относительно удалёнными друг от друга в первичной структуре аминокислотами или разными цепями белка, а не близко расположенными, как имеет место в α-спирали.
В некоторых белках β-структуры могут формироваться за счет образования водородных связей между атомами пептидного остова разных полипептидных цепей.
Полипептилные цепи или их части могут формировать параллельные или антипараллельные β-структуры. Если связанные несколько цепей полипептида направлены противоположно, а N- и С-концы не совпадают, то возникает антипараллельная β–структура, если совпадают – параллельная β-структура.
Другое название β-структур — β-листы (β-складчатые слои, β-sheets). β-лист формируется из двух или более β-структурных участков полипептидной цепи, называемых β-тяжами (β-strands). Обычно β-листы встречаются в глобулярных белках и содержат не более, чем 6 β-тяжей.
β-тяжи (β- strands)— это участки молекулы белка, в которых связи пептидного остова нескольких идущих подряд полипептидов организованы в плоской конформации. На иллюстрациях, β-тяжи белков иногда изображаются в виде плоских "лент со стрелками", чтобы подчеркнуть направление полипептидной цепи.
Основная часть β-тяжей расположена по соседству с другими тяжами и образует с ними обширную систему водородных связей между C=O и N-H группами основной белковой цепи (пептидного остова). β-тяжи могут быть упакованы <in a side-by-side manner>, будучи стабилизированными поперечно двумя или тремя водородными связями между последовательными тяжами. Такой способ укладки и называется β-листом.
Беспорядочный клубок — это участок пептидной цепи, который не имеет какой-либо правильной, периодической пространственной организации. Такие участки в каждом белке имеют свою фиксированную конформацию, которая определяется аминокислотным составом этого участка, а также вторичной и третичной структурами смежных областей, окружающих «беспорядочный клубок». В областях беспорядочного клубка пептидная цепь может сравнительно легко изгибаться, изменять конформацию, в то время как α-спирали и β-складчатый слой представляют собой достаточно жесткие структуры
Еще одна форма вторичной структуры обозначается как β-поворот. Эту структуру образуют 4 или больше аминокислотных остатка с водородной связью между первым и последним, причем таким образом, что пептидная цепь меняет направление на 180°. Петлевая структура такого поворота стабилизирована водородной связью между карбонильным кислородом аминокислотного остатка в начале поворота и N-H группой третьего по ходу цепи остатка в конце поворота.
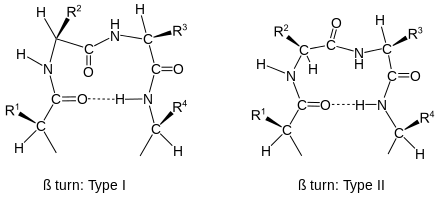
Если к β-повороту с двух концов подходят антипараллельные β-тяжи, то образуется вторичная структура, называемая β-шпилькой (β-hairpin)
Третичная структура белка (tertiary structure of protein) — В растворе при физиологических условиях полипептидная цепь сворачивается в компактное образование, имеющее определенную пространственную структуру, которую называют третичной структурой белка. Она образуется в результате самоукладки за счет взаимодействия между радикалами (ковалентные и водородные связи, ионные и гидрофобные взаимодействия). Впервые Т.с.б. была установлена для белка миоглобина Дж. Кендрю и М. Перуцем в 1959 г. (Нобелевская премия за 1962 г.). Т.с.б. практически полностью определяется первичной структурой белка. В настоящее время с помощью методов рентгеноструктурного анализа и ядерной магнитной спектроскопии (ЯМР-спектроскопия) определены пространственные (третичные) структуры большого числа белков.
Четвертичная структура белка. Белки, состоящие из одной полипептидной цепи, имеют только третичную структуру. Однако некоторые белки построены из нескольких полипептидных цепей, каждая из которых имеет третичную структуру. Для таких белков введено понятие четвертичной структуры, которая представляет собой организацию нескольких полипептидных цепей с третичной структурой в единую функциональную молекулу белка. Такой белок с четвертичной структурой называется олигомером, а его полипептидные цепи с третичной структурой — протомерами или субъединицами.
Конъюгат (conjugate, лат. conjugatio — соединение) - искусственно синтезированная (химически или путем рекомбинации in vitro) гибридная молекула, в которой соединены (объединены) две молекулы с разными свойствами; широко используется в медицине и экспериментальной биологии.
Гаптены
Гаптены - это «неполноценные антигены» (термин предложен иммунологом К. Ландштейнером). При введении в организм в нормальных условиях гаптены не способны индуцировать в организме иммунный ответ, так как обладают крайне низкой иммуногенностью.
Чаще всего гаптенами являются низкомолекулярные соединения (молекулярная масса меньше 10 кДа). Они распознаются организмом реципиента как генетически чужеродные (т.е. обладают специфичностью), но в силу низкой молекулярной массы сами по себе не вызывают иммунных реакций. Однако свойство антигенности они не утратили, что позволяет им специфически взаимодействовать с уже готовыми факторами иммунитета (антителами, лимфоцитами).
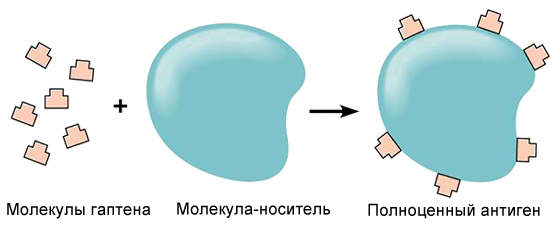
При определенных условиях удается за ставить иммунную систему макроорганизма специфически реагировав на гаптен как на полноценный антиген. Для этого необходимо искусственно укрупнить молекулу гаптена — соединить ее прочной связью с достаточно большой белковой молекулой или другим полимером-носителем. Синтезированный таким образом конъюгат будет обладать всеми свойствами полноценного антигена и вызывать иммунный ответ при введении в организм.
Эпитопы (антигенные детерминанты)
Организм способен образовать антитела почти к любой части молекулы антигена, но при нормальном иммунном ответе этого обычно не происходит. Комплексные антигены (белки, полисахариды) имеют особые участки, на которые собственно и формируется специфический иммунный ответ. Такие участки получили название эпитопы (epitope), от греч. epi — на, над, сверх и topos — место, местность. Синоним — антигенная детерминанта.
Эти участки состоят из немногих аминокислот или углеводов, каждый участок — это группа аминокислотных остатков белкового антигена или участок полисахаридной цепи. Эпитопы способны взаимодействовать как со специфическими рецепторами лимфоцитов, индуцируя тем самым иммунный ответ, так и с антигенсвязывающими центрами специфических антител.

Эпитопы разнообразны по своей структуре. Антигенной детерминантой (эпитопом) может быть участок поверхности белка, образованный радикалами аминокислот, гаптен или простетическая группа белка (связанный с белком небелковый компонент), особенно часто — полисахаридные группы гликопротеинов.
Антигенные детерминанты или эпитопы — это определенные участки трехмерной структуры антигенов. Существуют разные типы эпитопов — линейные и конформационные.
Линейные эпитопы образованы линейной последовательностью аминокислотных остатков.
В результате изучения строения белков было выяснено, что белковые молекулы имеют сложную пространственную структуру. При свертывании (в клубок) макромолекулы белка могут сближаться остатки, отдаленные друг от друга в линейной последовательности, образуя конформационную антигенную детерминанту.
Кроме того, сушествуют концевые эпитопы (расположенные на концевых участках молекулы антигена) и центральные. Определяют также «глубинные», или скрытые, антигенные детерминанты, которые проявляются при разрушении антигена.
Молекулы большинства антигенов имеют довольно большие размеры. Одна макромолекула белка (антиген), состоящая из нескольких сот аминокислот, может содержать много различных эпитопов. Некоторые белки могут иметь одну и ту же антигенную детерминанту в нескольких экземплярах (повторные антигенные детерминанты).
Против одного эпитопа образуется широкий спектр разных антител. Каждый из эпитопов способен стимулировать продукцию различных специфичных антител. К каждому из эпитопов могут вырабатываться специфические антитела.
Существует явление иммунодоминантности, которое проявляется в том, что эпитопы различаются по способности индуцировать иммунный ответ.
Не все эпитопы в составе белка характеризуются равной антигенностью. Как правило, некоторые эпитопы антигена обладают особой антигенностью, что проявляется в преимущественном образовании антител против этих эпитопов. Устанавливается иерархия в спектре эпитопов молекулы белка — некоторые из эпитопов являются доминирующими и большинство антител образуется именно к ним. Такие эпитопы названы иммунодоминантными эпитопами. Они почти всегда расположены на выдающихся частях молекулы антигена.
Строение антител (иммуноглобулинов)
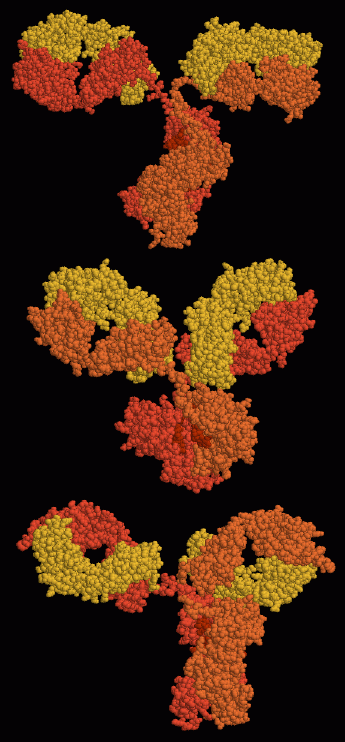 Иммуноглобулины IgG на основании экспериментальных данных. Каждый аминокислотный остаток молекулы белка изображен в виде маленького шарика. Визуализация построена с помощью программы RasMol.
Иммуноглобулины IgG на основании экспериментальных данных. Каждый аминокислотный остаток молекулы белка изображен в виде маленького шарика. Визуализация построена с помощью программы RasMol.В течение XX века биохимики стремились выяснить, какие варианты иммуноглобулинов существуют и какова структура молекул этих белков. Структура антител устанавливалась в ходе разнообразных экспериментов. В основном они заключались в том, что антитела обрабатывались протеолитическими ферментами (папаином, пепсином), и подвергались алкилированию и восстановлению меркаптоэтанолом.
Затем исследовались свойства полученных фрагментов: определялась их молекулярная масса (хроматографией), четвертичная структура (рентгеноструктурным анализом), способность связываться с антигеном и т.п. Также использовались антитела к данным фрагментам: выяснялось, могут ли антитела к одному типу фрагментов связываться с фрагментами другого типа. На основе полученных данных была построена модель молекулы антител.
Более 100 лет исследований структуры и функций иммуноглобулинов только подчеркнули сложную природу этих белков. В настоящее время, строение молекул иммуноглобулинов человека не описано полностью. Большинство исследователей сконцентрировали свои усилия не на описании структуры этих белков, а на выяснении механизмов, посредством которых антитела взаимодействуют с антигенами. Кроме того, молекулы антител <are very flexible>, поэтому изучение антител, сохраненных в неизменном виде, становится сложной задачей. Гораздо чаще удается выяснить точное строение отдельных фрагментов антител.
Несмотря на предполагаемое разнообразие иммуноглобулинов, их молекулы удалось классифицировать по структурам, входящим в эти молекулы. Эта классификация основана на том, что иммуноглобулины всех классов построены по общему плану, имеют некое универсальное строение.
Молекулы иммуноглобулинов - это сложные пространственные образования. Все без исключения антитела принадлежат к одному типу белковых молекул, имеющих глобулярную вторичную структуру, что соответствует их названию — «иммуноглобулины» (вторичная структура белка - это способ укладки в пространстве его полипептидной цепи). Они могут быть мономерами либо полимерами, построенными из нескольких субъединиц.
Тяжелые и легкие полипептидные цепи в структуре иммуноглобулинов
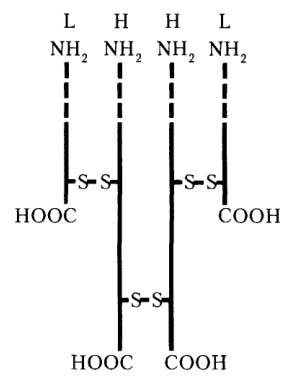 Пептидные цепи иммуноглобулинов. Схематическое изображение. Вариабельные области выделены пунктиром.
Пептидные цепи иммуноглобулинов. Схематическое изображение. Вариабельные области выделены пунктиром.Структурная единица иммуноглобулина — мономер, молекула состоящая из полипептидных цепей, соединенных друг с другом дисульфидными связями (S—S мостиками).
Если молекулу Ig обработать 2-меркаптоэтанолом (реактивом, разрушающим дисульфидные связи), то она распадется на пары полипептидных цепей. Полученные полипептидные цепи классифицируют по молекулярной массе: легкие и тяжелые. Лёгкие цепи имеют низкую молекулярную массу (около 23 кД) и обозначаются буквой L, от англ. Light —
лёгкий. Тяжёлые цепи Н (от англ.
Heavy — тяжёлый) имеют высокую молекулярную массу (варьирует в пределах 50 - 73 кД).
Так называемый мономерный иммуноглобулин содержит две L-цепи и две H-цепи. Легкие и тяжелые цепи удерживаются вместе дисульфидными мостиками. Дисульфидные связи соединяют легкие цепи с тяжелыми, а также тяжелые цепи между собой.
Основной структурной субъединицей всех классов иммуноглобулинов является пара «легкая цепь - тяжелая цепь» (L-H). Структура иммуноглобулинов разных классов и подклассов различается по числу и расположению дисульфидных связей между тяжелыми цепями, а также по числу (L-H)-субъединиц в молекуле. Н-цепи скрепляются различным числом дисульфидных связей. Типы тяжелых и легких цепей, входящих в состав разных классов иммуноглобулинов, также различаются.
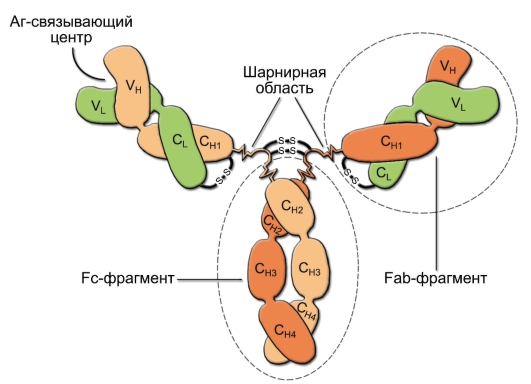
На рисунке представлена схема организации IgG в качестве типичного иммуноглобулина. Как и все иммуноглобулины, IgG содержит две одинаковые тяжелые (Н) цепи и две одинаковые легкие (L) цепи, которые объединены в четырехцепочечную молекулу посредством межцепьевых дисульфидных связей (-S-S-). Единственная дисульфидная связь, соединяющая Н- и L-цепи, локализуется недалеко от С-конца легкой цепи. Между двумя тяжелыми цепями также есть дисульфидная связь.
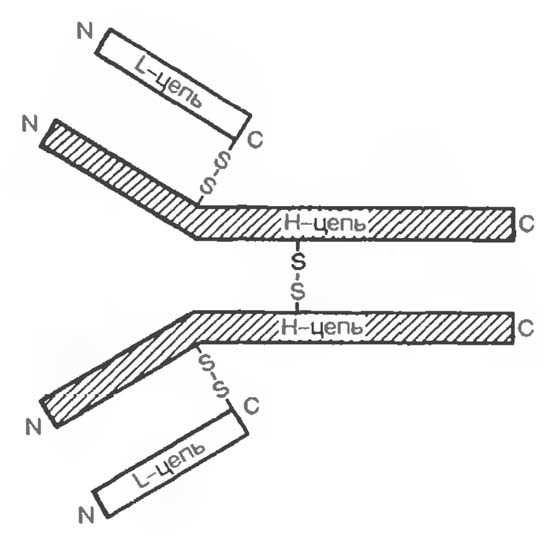
Домены в составе молекулы антитела
Легкие и тяжелые полипептидные цепи в составе молекулы Ig имеют определенную структуру. Каждая цепь условно разделена на специфические участки, называемые доменами.
Как легкие, так и тяжелые цепи не представляют собой прямолинейную нить. Внутри каждой цепи через регулярные и примерно равные промежутки по 100—110 аминокислот существуют дисульфидные мостики, которые формируют петли в структуре каждой цепи. Наличие дисульфидных мостиков означает, что каждая петля в пептидных цепях должна формировать компактно сложенный глобулярный домен. Таким образом, каждая полипептидная цепь в составе иммуноглобулина образует несколько глобулярных доменов в виде петель, включающих примерно по 110 аминокислотных остатков.
Можно сказать, что молекулы иммуноглобулинов собраны из отдельных доменов, каждый из которых располагается вокруг дисульфидного мостика и гомологичен остальным.
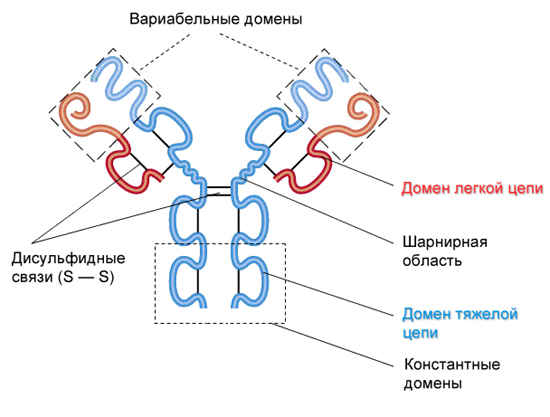
В каждой из легких цепей молекул антител существуют две внутрицепочечные дисульфидные связи, соответственно каждая легкая цепь имеет по два домена. Число таких связей в тяжелых цепях различно; тяжелые цепи содержат по четыре или пять доменов. Домены разделены несложно организованными отрезками. Наличие таких конфигураций было подтверждено прямыми наблюдениями и с помощью генетического анализа.
Первичная, вторичная, третичная и четвертичная структура иммуноглобулинов
Строение молекулы иммуноглобулина (как и других белков) определяется первичной, вторичной, третичной и четвертичной структурой. Первичная структура -— это последовательность аминокислот, составляющих легкие и тяжелые цепи иммуноглобулинов. Рентгеноструктурный анализ показал, что легкие и тяжелые цепи иммуноглобулинов состоят из компактных глобулярных доменов (так называемых иммуноглобулиновых доменов). Домены уложены в характерную третичную структуру, названную иммуноглобулиновой укладкой (immunoglobulin fold).
Иммуноглобулиновые домены — это области в третичной структуре молекулы Ig, которым свойственна определенная автономия структурной организации. Домены формируются различными отрезками одной и той же полипептидной цепи, свернутыми в «клубки» (глобулы). В глобулу включается примерно 110 аминокислотных остатков.
Домены имеют сходную с друг другом общую структуру и определенные функции. Внутри доменов пептидные фрагменты, входящие в состав домена, образуют компактно уложенную антипараллельную β-складчатую структуру, стабилизированную водородными связями (вторичная структура белка). Участков с α-спиральной конформацией в структуре доменов практически не содержится.
Вторичная структура каждого из доменов сформирована посредством укладки протяженной полипептидной цепи back and forth upon itself в два антипараллельных β-слоя (β-листа), содержащих несколько β-складок. Каждый β-лист имеет плоскую форму — полипептидные цепи в β-складках почти полностью вытянуты.
Два β-листа, из которых состоит иммуноглобулиновый домен, уложены в структуру, названную β-сэндвичем ("словно два куска хлеба друг на друга"). Структура каждого иммуноглобулинового домена стабилизирована за счет внутридоменной дисульфидной связи — β-листы ковалентно связаны дисульфидной связью между цистеиновыми остатками каждого β-листа. Каждый β-лист состоит из антипараллельных β-тяжей, соединенных петлями различной длины.
Домены, в свою очередь, связаны между собой продолжением полипептидной цепи, которая продолжается за пределы β-складчатых листов. Имеющиеся между глобулами открытые участки полипептидной цепи особенно чувствительные к протеолитическим ферментам.
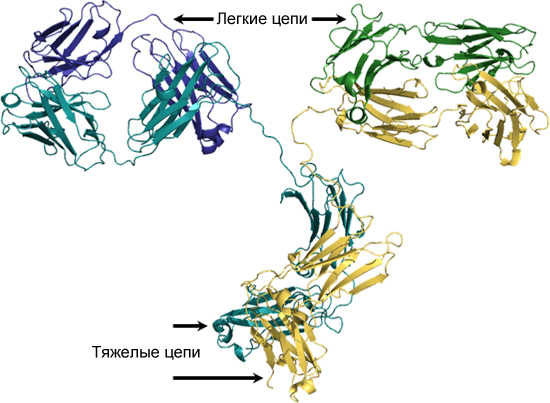
Глобулярные домены пары из легкой и тяжелой цепи взаимодействуют между собой, образуя четвертичную структуру. Благодаря этому формируются функциональные фрагменты, которые позволяют полекуле антитела специфически связывать антиген и, в то же время, выполнять ряд биологических эффекторных функций.
Вариабельные и постоянные домены
Домены в пептидных цепях отличаются по постоянству аминокислотного состава. Различают вариабельные и постоянные домены (области). Вариабельные домены обозначаются буквой V, от англ. variable - «изменчивый» и называются V-доменами. Постоянные (константные) домены обозначают буквой C, от англ constant - «постоянный» и называют С-доменами.
Иммуноглобулины, продуцируемые разными клонами плазматических клеток, имеют разные по аминокислотной последовательности вариабельные домены. Константные домены сходны или очень близки для каждого изотипа иммуноглобулина.
Каждый домен обозначают буквой, означающей его принадлежность к легкой или тяжелой цепи, и числом, указывающим его положение.
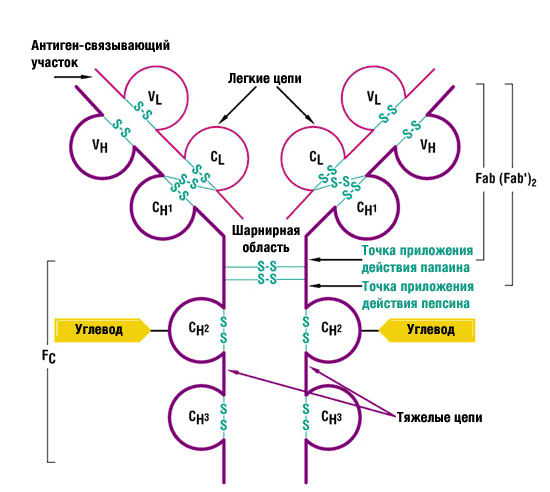
Первый домен на легкой и тяжелой цепях всех антител крайне вариабелен по последовательности аминокислот; он обозначается как VL и VH соответственно.
Второй и последующие домены на обеих тяжелых цепях гораздо более постоянны по последовательности аминокислот. Они обозначаются CH или СH1, СH2 и СH3. Иммуноглобулины IgM и IgЕ имеют дополнительный СH4-домен на тяжелой цепи, расположенный за доменом СH3.
Половину легкой цепи, включающую карбоксильный конец, называют константной областью CL, a N-концевую половину легкой цепи – вариабельной областью VL.
С доменом СН2 также связаны цепочки углеводов. Иммуноглобулины разных классов сильно отличаются по количеству и расположению углеводных групп. Углеводные компоненты иммуноглобулинов имеют сходное строение. Они состоят из постоянного ядра и вариабельной наружной части. Углеводные компоненты влияют на биологические свойства антител.
Fab- и Fc-фрагменты молекулы иммуноглобулина
Вариабельные домены легкой и тяжелой цепи (VH и VL) вместе с ближайшими к ним константными доменами (СH1 и CL1) образуют Fab-фрагменты антител (fragment, antigen binding). Участок иммуноглобулина, связывающийся со специфическим антигеном, формируется N-концевыми вариабельными областями легких и тяжелых цепей, т.е. VH - и VL -доменами.
Остальную часть, представленную C-концевыми константными доменами тяжелых цепей, обозначают как Fc-фрагмент (fragment, crystallizable). Fc-фрагмент включает остальные CH -домены, скрепленные дисульфидными связями. В месте соединения Fab- и Fc-фрагментов расположена шарнирная область, позволяющая антиген-связывающим фрагментам разворачиваться для более тесного контакта с антигеном.
Шарнирная область
На границе Fab- и Fc-фрагментов располагается т.наз. «шарнирная область», имеющая гибкую структуру. Она обеспечивает подвижность между двумя Fab-фрагментами Y-образной молекулы антитела. Подвижность фрагментов молекулы антитела друг относительно друга — это важная структурная характеристика иммуноглобулинов. Такой тип межпептидного соединения придает структуре мoлeкyлы динамичность — он позволяет легко менять конформацию в зависимости от окружающих условий и состояния.
Шарнирная область — это участок тяжелой цепи. Шарнирная область содержит дисульфидные связи, соединяющие тяжелые цепи между собой. У каждого класса иммуноглобулинов шарнирная область имеет свое строение.
У иммуноглобулинов (возможно, за исключением IgM и IgE) шарнирная область состоит из короткого сегмента аминокислот и обнаруживается между участками СH1 и СH2 тяжелых цепей. Этот сегмент состоит преимущественно из остатков цистеина и пролина. Цистеины вовлечены в формирование дисульфидных мостиков между цепями, а пролиновые остатки предотвращают складывание в глобулярную структуру.
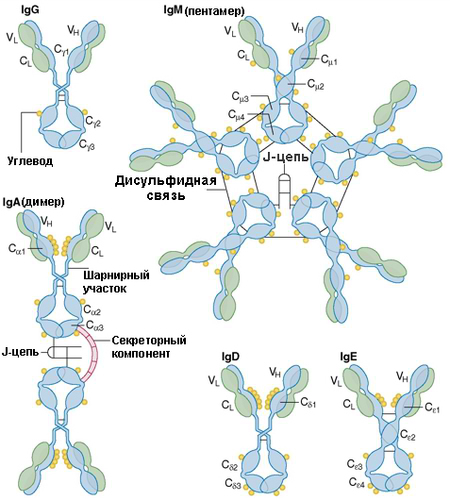
Типичное строение молекулы иммуноглобулина на примере IgG
Схематическое изображение на плоском рисунке неточно отражает структуру Ig; в действительности вариабельные домены легкой и тяжелой цепей не располагаются параллельно, а тесно, крест-накрест переплетены друг с другом.
Типичное строение иммуноглобулина удобно рассмотреть на примере молекулы антитела класса IgG. Всего в молекуле IgG 12 доменов — по 4 на тяжелых цепях и по 2 на легких цепях.
В состав каждой легкой цепи входит два домена – один вариабельный (VL , variable domain of the light chain) и один константный (CL, constant domain of the light chain). В состав каждой тяжелой цепи – один вариабельный (VH , variable domain of the heavy chain) и три константных домена (CH 1–3, constant domains of the heavy chain). Примерно четвертую часть тяжелой цепи, включающую N-конец, относят к вариабельной области Н-цепи (VH ), остальная часть ее – это константные области (СН1, СН2, СН3).
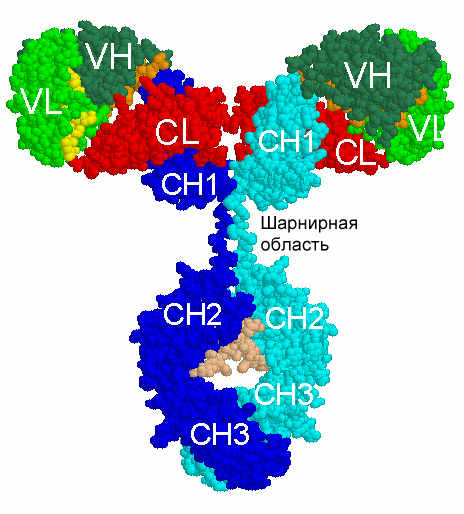
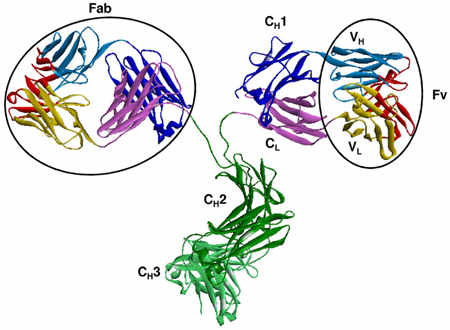
Каждая пара вариабельных доменов VH и VL, расположенных в соседних тяжелой и легкой цепях, образует вариабельный фрагмент (Fv, variable fragment).
Типы тяжелых и легких цепей в составе молекул антител
По различиям первичной структуры постоянных областей цепи делятся на типы. Типы определяются первичной аминокислотной последовательностью цепей и степенью их гликозилирования. Легкие цепи делятся на два типа: κ и λ (каппа и лямбда), тяжелые — на пять типов: α, γ, μ, ε и δ (альфа, гамма, мю, эпсилон и дельта). Среди многообразия тяжелых цепей альфа-, мю- и гамма-типов выделяют подтипы.
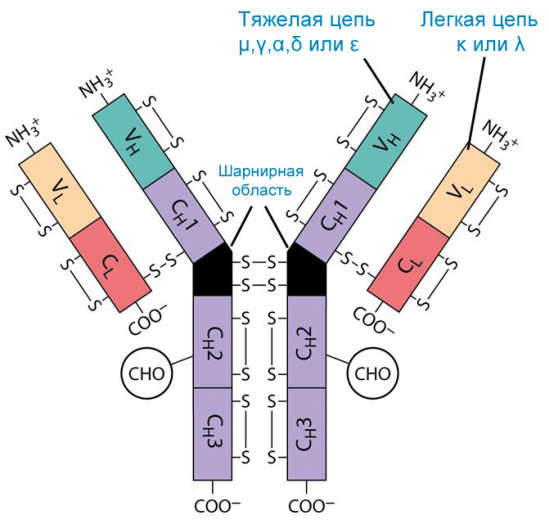
Классификация иммуноглобулинов
Иммуноглобулины классифицируют по типу H-цепей (тяжелых цепей). Постоянные области тяжелых цепей у иммуноглобулинов разных классов неодинаковы. Иммуноглобулины человека поделены на 5 классов и ряд подклассов, по типам тяжелых цепей, которые входят в их состав. Эти классы получили название IgA, IgG, IgM, IgD и IgE.
Сами Н-цепи обозначены греческой буквой, соответствующей большой латинской букве названия одного из иммуноглобулинов. У IgA тяжелые цепи α (альфа), IgM – μ (мю), IgG – γ (гамма), IgE – ε (эпсилон), IgD – δ (дельта).
У иммуноглобулинов IgG, IgM и IgA имеется ряд подклассов. Разделение на подклассы (субтипы) также происходит в зависимости от особенностей Н-цепей. У человека существует 4 подкласса IgG: IgG1, IgG2, IgG3 и IgG4, содержащие тяжелые цепи γ1, γ2, γ3 и γ4 соответственно. Эти H-цепи отличаются небольшими деталями Fc-фрагмента. Для μ-цепи известны 2 подтипа— μ1- и μ2-. IgA имеет 2 подкласса: IgA1 и IgA2 с α1- и α2-подтипами α-цепей.
В каждой молекуле иммуноrлобулина все тяжелые цепи относяrся к одинаковому типу, в соответствии с классом или подклассом.
Все 5 классов иммуноглобулинов состоят из тяжелых и легких цепей.
Легкие цепи (L-цепи) у иммуноглобулинов разных классов одни и те же. У всех иммуноглобулинов легкие цепи могут быть или обе κ (каппа) или обе λ (лямбда). Иммуноглобулины всех классов разделяют на К- и L-типы, в зависимости от присутствия в составе их молекул легких цепей κ- или λ-типов, соответственно. У человека соотношение K- и L-типов составляет 3:2.
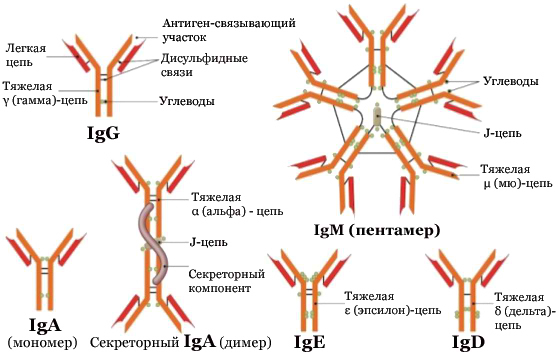
Классы и подклассы, вместе взятые, называют изотипами иммуноглобулинов. Изотип антител (класс, подкласс иммуноглобулинов – IgM1, IgM2, IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgD, IgE) определяется C-доменами тяжелых цепей.
Каждый класс включает огромное множество индивидуальных иммуноглобулинов, различающихся по первичной структуре вариабельных областей; общее число иммуноглобулинов всех классов равно ≈ 10^7.
Строение молекул антител различных классов
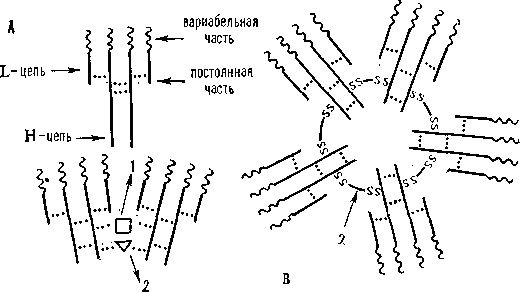
Схемы строения иммуноглобулинов. (А) — мономерные IgG, IgE, IgD, IgA; (Б) — полимерный секреторный Ig A (slgA) и IgM (В); (1) — секреторный компонент; (2) — соединительная J-цепь.
1. Классы антител IgG, IgD и IgE
Молекулы антител классов IgG, IgD и IgE мономерны; они имеют Y-образную форму.
На долю иммуноглобулинов класса IgG приходится 75% от общего количества имуноглобулинов человека. Находятся они как в крови, так и вне сосудов. Важным свойством IgG является их способность проходить через плаценту. Таким образом материнские антитела попадают в организм новорожденного ребенка и защищают его от инфекции в первые месяцы жизни (естественный пассивный иммунитет).
IgD в основном находятся на мембране В-лимфоцитов. Имеют строение, подобное IgG, 2 активных центра. Тяжелая цепь (δ-цепь) состоит из вариабельного и 3 константных доменов. Шарнирная область δ-цепи самая длинная, локализация углеводов в этой цепи также необычна.
IgЕ – концентрация этого класса иммуноглобулинов в сыворотке крови чрезвычайно низкая. Молекулы IgЕ в основном фиксированы на поверхности тучных клеток и базофилов. По своему строению IgЕ сходен с IgG, имеет 2 активных центра. Тяжелая цепь (ε-цепь) имеет один вариабельный и 4 константных домена. Предполагается, что IgЕ имеет существенное значение в развитии антигельминтозного иммунитета. IgЕ играет главную роль в патогенезе некоторых аллергических заболеваний (бронхиальная астма, сенная лихорадка) и анафилактического шока.
2. Классы антител IgM и IgA
Иммуноглобулины IgM и IgA формируют полимерные структуры. Для полимеризации IgM и IgA включают в свой состав дополнительную полипептидную цепочку с молекулярной массой 15 кД, называемую J-цепью (joint-связь, от англ. joining – соединение). Эта J-цепь связывает терминальные цистеины на С-концах соответственно тяжелых μ- и α -цепей IgM и IgA.
На поверхности зрелых B-лимфоцитов молекулы IgM располагаются в виде мономеров. Однако в сыворотке они существуют в виде пентамеров: молекула IgM состоит из пяти структурных молекул, расположеных радиально. Пентамер IgM сформирован из пяти мономеров-«рогаток», подобных IgG, соедененных между собой дисульфидными связями и J-цепью. Их Fc-фрагменты направлены в центр (где и соединены J-цепью), а Fab-фрагменты - наружу.
В IgM тяжелые (Н) цепи состоят из 5 доменов, так как содержат 4 константных домена. Тяжелые цепи IgM не имеют шарнирной области; её роль выполняет домен СH2, обладающий некоторой конформационной лабильностью.
IgM синтезируется в основном при первичном иммунном ответе и преимущественно содержится во внутрисосудистом русле. Количество Ig M в сыворотке крови здоровых людей составляет около 10% от общего количества Ig.
Антитела IgA построены из различного количества мономеров. Иммуноглобулины класса А делят на два вида: сывороточный и секреторный. Большая часть (80%) IgА, присутствующих в сыворотке крови, имеет мономерную структуру. Менее 20% IgA в сыворотке представлено димерными молекулами.
Секреторные IgA находятся не в крови, а в составе экзосекретов на слизистых оболочках и обозначаются sIgА. В секретах слизистых оболочек IgА представлены в виде димеров. Секреторный IgA формирует димер из двух «рогаток» (Ig-мономеров). С-концы тяжелых цепей в молекуле sIgА соединены между собой J-цепью и белковой молекулой, которая называется «секреторный компонент».
Секреторный компонент вырабатывается эпителиальными клетками слизистых оболочек. Он присоединяется к молекуле IgA в момент её прохождения через эпителиальные клетки. Секреторный компонент защищает sIgА от расщепления и инактивации протеолитическими ферментами, которые содержатся в большом количестве в секрете слизистых оболочек.
Основная функция sIgА – защита слизистых оболочек от инфекции. Роль sIgA в обеспечении местного иммунитета весьма значительна, т.к. общая площадь слизистых оболочек в организме взрослого человека составляет несколько сот квадратных метров и намного превышает поверхность кожи.
Высокая концентрация sIgА обнаруживается в женском грудном молоке, особенно в первые дни лактации. Они защищают желудочно-кишечный тракт новорожденного от инфекции.
Дети рождаются без IgA и получают его с молоком матери. Достоверно показано, что дети, находящиеся на естественном вскармливании, значительно реже болеют кишечными инфекциями и заболеваниями дыхательных путей по сравнению с детьми, получающими искусственное питание.
Антитела класса IgА составляют 15-20% от общего содержания иммуноглобулинов. IgА не проникают через плацентарный барьер. Ig A синтезируется плазматическими клетками, находящимися преимущественно в подслизистых тканях, на слизистой эпителиальной поверхности дыхательных путей, урогенитального и кишечного тракта, почти во всех экскреторных железах. Часть Ig А попадает в общую циркуляцию, но большая его часть секретируется местно на слизистых оболочках в виде sIgA и служит местным защитным иммунологическим барьером слизистых. Сывороточный IgA и sIgA это различные иммуноглобулины, sIgA нет в сыворотке крови.
У лиц с иммунодефицитом IgA отмечается склонность к аутоиммунным заболеваниям инфекциям дыхательных путей, гайморовых и лобных пазух, кишечным расстройствам.
Расщепление молекулы иммуноглобулина ферментами
Протеолитические ферменты (такие, как папаин или пепсин) расщепляют молекулы иммуноглобулинов на фрагменты. При этом под воздействием разных протеаз можно получить различные продукты. Полученные таким способом фрагменты иммуноглобулинов можно использовать для исследовательских, либо медицинских целей.
Глобулярная структура иммуноглобулинов и способность ферментов расщеплять эти молекулы на крупные составляющие в строго определенных местах, а не разрушать их до олигопептидов и аминокислот, указывает на чрезвычайную компактность структуры.
1. Расщепление молекулы иммуноглобулина папаином. Fab- и Fc-фрагменты антител.
В конце 50-х — начале 60-х годов, английский ученый Р.Р. Портер проанализировал структурные характеристики антител IgG, посредством разделения их молекулы папаином (очищенным ферментом сока папайи). Папаин разрушает иммуноглобулин в шарнирной области, выше межцепьевых дисульфидных связей. Этот фермент расщепляет молекулу иммуноглобулина на три фрагмента, примерно одинаковых размеров.
Два из них получили название Fab-фрагментов (от англ. fragment antigen-binding — фрагмент антигенсвязывающий). Fab-фрагменты полностью идентичны и, как показали исследования, предназначены для связывания с антигеном. Участок тяжелой цепи в составе Fab-фрагмента называют Fd; он состоит из доменов VH и СH1.
Третий фрагмент может быть выкристаллизован из раствора и не может связывать антиген. Этот фрагмент назван Fc-фрагментом (от англ. fragment crystallizable — фрагмент кристализации). Он отвечает за биологические функции молекулы антитела после связывания антигена и Fab-части неповрежденной молекулы антитела.
Fc-фрагмент имеет одинаковую структуру у антител каждого класса и подкласса и разную — у антител, принадлежащих к разным подклассам и классам.
Fc-фрагмент молекулы взаимодействует с клетками иммунной системы: нейтрофилами, макрофагами и другими мононуклеарными фагоцитами , несущими на своей поверхности рецепторы для Fc-фрагмента. Если антитела связались с патогенными микроорганизмами, они могут своим Fc-фрагментом взаимодействовать и с фагоцитами. Благодаря этому клетки возбудителя будут разрушены этими фагоцитами. Фактически антитела действуют в данном случае как молекулы-посредники.
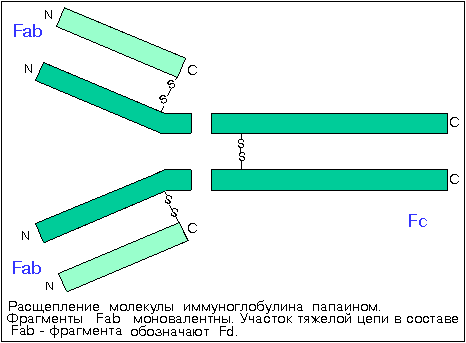
Впоследствии стало известно, что Fc-фрагменты иммуноглобулинов в пределах одного изотипа у данного организма строго идентичны независимо от специфичности антитела по антигену. За эту инвариантность их стали называть константными областями (fragment constant — Fc, аббревиатура совпала).
2. Расщепление молекулы иммуноглобулина пепсином.
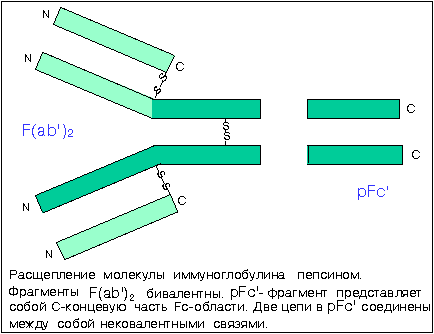
Другой протеолитический фермент — пепсин — расщепляет молекулу в другом месте, ближе к С-концу Н-цепей, чем это делает папаин. Расщепление происходит «ниже» дисульфидных связей, скрепляющих Н-цепи. В результате при действии пепсина образуется двухвалентный антигенсвязывающий F(аb')2 -фрагмент и укороченный pFc'-фрагмент. Фрагмент pFc' представляет собой C-концевую часть Fc -области.
Пепсин отсекает pFc' -фрагмент от большого фрагмента с константой седиментации 5S. Этот большой фрагмент получил название F(ab')2 , поскольку он, как и исходное антитело, бивалентен в отношении связывания антигена. Он представляет собой соединенные Fab-фрагменты, связанные дисульфидным мостиком в шарнирной области. Эти Fab-фрагменты одновалентны и гомологичны с папаиновыми Fab-фрагментами I и II, но их Fd-фрагмент примерно на десять аминокислотных остатков больше.
Антигенсвязывающие центры антител (паратопы)
В Fab-фрагмент иммуноглобулина входят V-домены обеих цепей, CL и CH1-домены. Антигенсвязывающий участок Fab-фрагмента получил несколько названий: активный или антигенсвязывающий центр антител, антидетерминанта или паратоп.
В образовании активных центров участвуют вариабельные отрезки легких и тяжелых цепей . Активный центр представляет собой щель, расположенную между вариабельными доменами легкой и тяжелой цепей. В формировании активного центра участвуют оба этих домена.
 Молекула иммуноглобулина. L - лёгкие цепи; H - тяжёлые цепи; V - вариабельная область; С - константная область; N-концевые области L- и Н-цепей (V-область) образуют два антигенсвязывающих центра в составе Fab-фрагментов.
Молекула иммуноглобулина. L - лёгкие цепи; H - тяжёлые цепи; V - вариабельная область; С - константная область; N-концевые области L- и Н-цепей (V-область) образуют два антигенсвязывающих центра в составе Fab-фрагментов. Каждый Fab-фрагмент иммуноглобулинов IgG имеет один антигенсвязывающий центр. Активные центры антител других классов, способные взаимодействовать с антигеном, также расположены в Fab-фрагментах. Антитела IgG, IgA и IgE имеют по 2 активных центра, IgM — по 10 центров.
Иммуноглобулины могут связывать антигены разной химической природы: пептиды, карбогидраты, сахара, полифосфаты, стероидные молекулы.
Существенным и уникальным свойством антител является их способность вступать в связывание с цельными, нативными молекулами антигенов, непосредственно в том виде, в каком антиген проник во внутреннюю среду организма. Для этого не требуется никакая предварительная метаболическая обработка антигенов
Структура доменов в составе молекул иммуноглобулинов
Вторичная структура полипептидных цепей молекулы иммуноглобулина обладает доменным строением. Отдельные участки тяжелых и легких цепей свернуты в глобулы (домены), которые соединены линейными фрагментами. Каждый домен имеет примерно цилиндрическую форму и представляет собой β-складчатую структуру, сформированную из антипараллельных β-складок. В рамках базовой структуры, между C- и V-доменами есть определенная разница, которую можно рассмотреть на примере легкой цепи.
На рисунке схематически изображена укладка одиночной полипептидной цепи белка Бенс-Джонса, содержащей VL и CL домены. Схема построена по данным рентгеноструктурного анализа — метода, который позволяет устанавливать трехмерную структуру белков. На схеме можно видеть сходства и различия между V- и C-доменами.
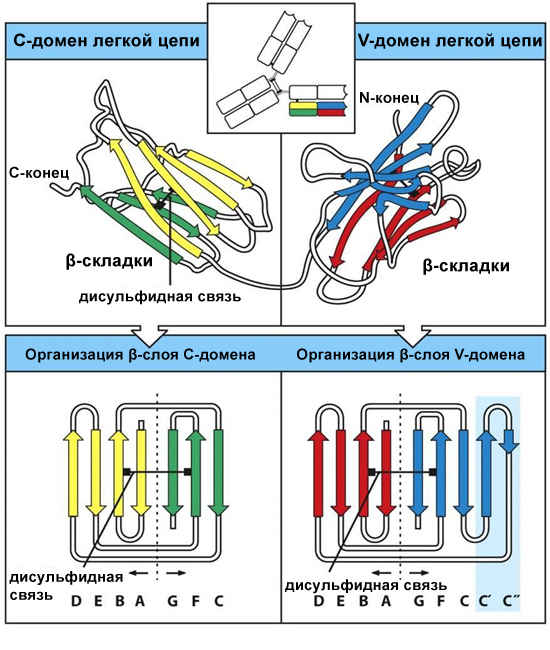
В верхней части рисунка схематически показана пространственная укладка постоянного (C) и вариабельного (V) доменов легкой цепи молекулы белка. Каждый домен - это цилиндрическая "бочкообразная" (barrel-shaped) структура, в которой участки полипептидной цепи (β-тяжи), идущие в противоположных направлениях (т.е. антипареллельные) упакованы так, что формируют два β-листа, удерживаемых вместе дисульфидной связью.
Каждый из доменов, V- и C-, состоит из двух β-листов (слоев с β-складчатой структурой). Каждый β-лист содержит несколько антипараллельных (идущих в противоположных направлениях) β-тяжей: в С-домене β-листы содержат четыре и три β-тяжа, в V-домене — оба слоя состоят из четырех β-тяжей. На рисунке β-тяжи показаны желтым и зеленым для C-домена и красным и синим для V-домена.
В нижней части рисунка иммуноглобулиновые домены рассмотрены подробнее. В этой половине картинки отображена схема взаимного расположения β-тяжей для V- и C-доменов легкой цепи. Можно яснее рассмотреть создающий итоговую структуру способ укладки их полипептидных цепей при формировании из них β-листов. Чтобы показать укладку, β-тяжи обозначены буквами латинского алфавита, в соответствии с порядком их появления в последовательности аминокислот, составляющих домен. Порядок следования в каждом β-листе — это характеристика иммуноглобулиновых доменов.
Основная разница между V- и C-доменами состоит в том, что V-домен больше и содержит дополнительные β-тяжи, обозначенные, как Cʹ и Cʹʹ. На рисунке β-тяжи Cʹ и Cʹʹ, имеющиеся у V-доменов, но отсутствующие у C-доменов выделены голубым прямоугольником. Можно видеть, что каждая полипептидная цепь формирует гибкие петли между последовательными β-тяжами при смене направления. В V-домене, гибкие петли, сформированные между некоторыми из β-тяжей, входят в структуру активного центра молекулы иммуноглобулина.
Гипервариабельные области в составе V-доменов
Уровень вариабельности внутри вариабельных доменов распределен неравномерно. Не весь вариабельный домен изменчив по своему аминокислотному составу, а лишь его малая часть — гипервариабельные области. На их долю приходится около 20 % аминокислотной последовательности V-доменов.
В структуре цельной молекулы иммуноглобулина VH- и VL-домены объединены. Их гипервариабельные области примыкают друг к другу и создают единый гипервариабельный участок в виде кармана. Это участок, который специфически связывается с антигеном. Гипервариабельные области определяют комплементарность антитела антигену.
Поскольку гипервариабельные участки играют ключевую роль в распознавании и связывании антигена, их еще называют участками, определяющими комплементарность — CDR (Сomplementarity determining regions). В вариабельных доменах тяжелой и легкой цепей выделяют по три CDR (VL CDR1–3, VH CDR1–3).
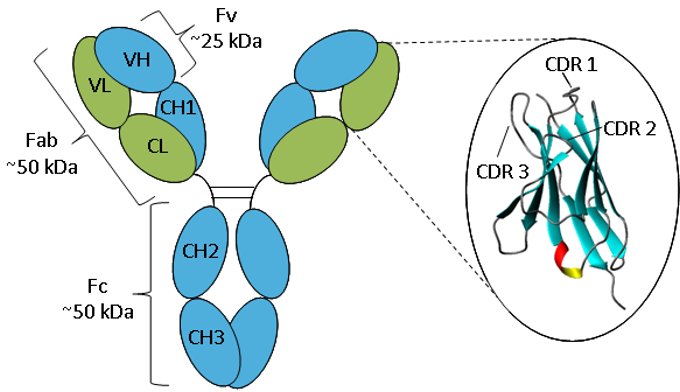
Между гипервариабельными областями расположены относительно постоянные участки аминокислотной последовательности, которые называются каркасными участками (framework region, FR). На их долю приходится около 80% аминокислотной последовательности V-доменов. Роль таких участков заключается в поддержании относительно однотипной трехмерной структуры V-доменов, которая необходима для обеспечения аффинного взаимодействия гипервариабельных участков с антигеном.
В последовательности вариабельного домена области 3 гипервариантные области чередуются с 4 относительно инвариантными «каркасными» участками FR1–FR4,
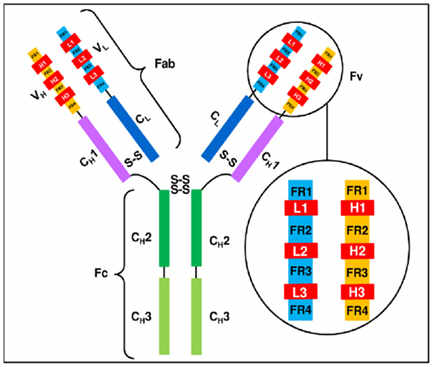
H1–3 – CDR-петли, входящие в состав цепей.
Особый интерес представляет пространственное расположение гипервариабельных областей в трех отдельных петлях вариабельного домена. Эти гипервариабельные области, хотя и находятся на большом отдалении друг от друга в первичной структуре легкой цепи, но, при образовании трехмерной структуры, они оказываются расположенными в непосредственной близости друг к другу.
В пространственной структуре V-доменов гипервариабельные последовательности расположены в зоне изгибов полипептидной цепи, направленной навстречу соответствующим участкам V-домена другой цепи (т.е. CDR легкой и тяжелой цепей направлены навстречу друг другу). В результате взаимодействия вариабельного домена H- и L-цепей и формируется антигенсвязывающий участок (активный центр) иммуноглобулина. По данным электронной микроскопии, он представляет собой полость длиной 6 нм и шириной 1,2–1,5 нм.
Пространственная структура этой полости, обусловленная строением гипервариабельных участков, определяет способность антител распознавать и связывать конкретные молекулы на основе пространственного соответствия (специфичность антител). В формирование активного центра вносят вклад и пространственно разделенные участки Н- и L-цепей. Гипервариабельные участки V-доменов входят в состав активного центра не полностью — поверхность антигенсвязывающего участка захватывает только около 30% CDR.
Гипервариабельные области тяжелой и легкой цепи определяют индивидуальные особенности строения антигенсвязывающего центра для каждого клона Ig и многообразие их специфичностей.
Сверхвысокая вариабельность CDR и активных центров обеспечивает уникальность молекул иммуноглобулинов, синтезируемых В-лимфоцитами одного клона, не только по структуре, но и по способности связывать различные антигены. Несмотря на то, что структура иммуноглобулинов довольно хорошо известна и именно CDR отвечают за их особенности, до сих пор не ясно, какой именно домен отвечает за связывание антигена в наибольшей степени.
Взаимодействие антител и антигенов (взаимодействие эпитопа и паратопа)
В основе реакции антиген—антитело лежит взаимодействие между эпитопом антигена и активным центром антитела, основанное на их пространственном соответствии (комплементарности). В результате связывания патогена с активным центром антитела происходит нейтрализация патогена и затрудняется его проникновение в клетки организма.
В процессе взаимодействия с антигеном принимает участие не вся молекула иммуноглобулина, а лишь ее ограниченный участок — антигенсвязывающий центр, или паратоп, который локализован в Fab-фрагменте молекулы Ig. При этом антитело взаимодействует не со всей молекулой антигена сразу, а лишь с ее антигенной детерминантой (эпитопом).
Активный центр антител является структурой, пространственно комплементарной (специфичной) детерминантой группе антигена. Активный центр антител обладает функциональной автономией, т.е. способен связывать антигенную детерминанту в изолированном виде.
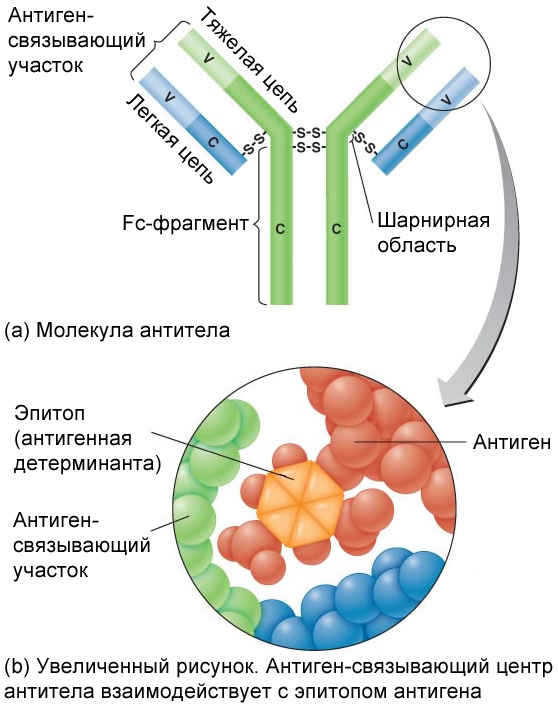
Со стороны антигена, за взаимодействие с активными центрами антигенраспознающих молекул ответственны эпитопы, которые взаимодействуют со специфичными антителами. Эпитоп непосредственно вступает в ионные, водородные, ван-дер-ваальсовы и гидрофобные связи с активным центром антитела.
Специфическое взаимодействие антител с молекулой антигена связано с относительно небольшим участком ее поверхности, соответствующим по размеру антиген-связывающему участку рецепторов и антител.
Связь антигена с антителом осуществляется за счет слабых взаимодействий в пределах антигенсвязывающего центра. Все эти взаимодействия проявляются только при близком контакте молекул. Такое маленькое расстояние между молекулами может быть достигнуто только за счет комплементарности эпитопа и активного центра антитела.
Перекрестная реактивность
Иногда один и тот же антигенсвязывающий центр молекулы антитела может связываться с несколькими различными антигенными детерминантами (обычно эти антигенные детерминанты очень схожи). Такие антитела называют перекрестно-реагирующими, способными к полиспецифическому связыванию.
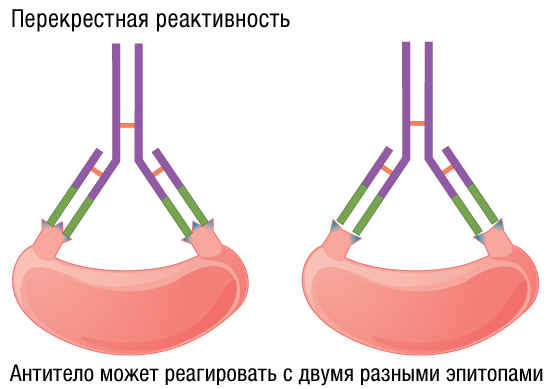
Например если антиген А имеет общие эпитопы с антигеном Б, то часть антител, специфичных к А, будет реагировать также с Б. Этот феномен назван перекрестной реактивностью.
Полные и неполные антитела. Валентность
Валентность – это количество активных центров антитела, которые способны соединяться с антигенными детерминантами. Антитела имеют различное число активных центров в молекуле, что и определяет их валентность. В связи с этим, различают полные и неполные антитела.
Полные антитела имеют не менее двух активных центров. Полные (двух- и пятивалентные) антитела при взаимодействии in vitro с антигеном, в ответ на который они выработаны, дают визуально видимые реакции (агглютинации, лизиса, преципитации, связывания комплемента и др.).
Неполные, или моновалентные антитела отличаются от обычных (полных) антител тем, что имеют лишь один активный центр, второй центр у таких антител не работает. Это не значит, что второй активный центр молекулы отсутствует. Второй активный центр у подобных иммуноглобулинов экранирован различными структурами, либо обладает низкой авидностью. Такие антитела могут взаимодействовать с антигеном, блокировать его, связывая эпитопы антигена и препятствуя контакту с ним полных антител, но не вызывают агрегацию антигена. Поэтому они также называются блокирующими.
Реакция между неполными антителами и антигеном не сопровождается макроскопическими феноменами. Неполные антитела при специфическом взаимодействии с гомологичным антигеном не дают видимого проявления серологической реакции, т.к. не могут аггрегировать частицы в крупные конгломераты, а лишь блокируют их.
Неполные антитела образуются независимо от полных и выполняют те же функции. Они также представлены различными классами иммуноглобулинов.
Идиотипы и идиотопы
Антитела являются сложными белковыми молекулами, которые сами по себе могут иметь антигенные свойства и вызывать образование антител. В их составе различают несколько типов антегенных детерминант (эпитипов): изотипы, аллотипы и идиотипы.
Различные антитела отличаются друг от друга своими вариабельными областями. Антигенные детерминанты вариабельных областей (V-областей) антител называются идиотопами. Идиотопы могут быть построены из характерных участков V-областей только лишь H-цепей или же L-цепей. В большинстве случаев, в образовании идиотопа участвуют обе цепи сразу.
Идиотопы могут относиться к антигенсвязывающему участку (сайт-ассоциированные идиотопы) или не иметь к нему отношения (неассоциированные идиотопы).
Сайт-ассоциированные идиотопы зависят от структуры антигенсвязывающего участка антитела (принадлежащего к Fab-фрагменту). Если этот участок занят антигеном, то антиидиотопическое антитело уже не может реагировать с антителом, имеющим данный идиотоп. Другие идиотопы, по-видимому, не имеют такой тесной связи с антигенсвязывающими участками.
Набор идиотопов на молекуле любого антитела обозначают как идиотип. Таким образом, идиотип состоит из набора идиотопов – антигенных детерминант V-области антитела.
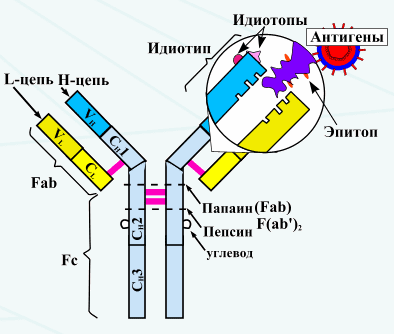
Групповые конституциональные варианты антигенной структуры тяжёлых цепей называются аллотипами. Аллотипы - детерминанты, кодируемые аллелями данного иммуноглобулинового гена.
Изотипы - детерминанты, по которым различаются классы и подклассы тяжелых цепей и варианты κ (каппа) и λ (лямбда) легких цепей.
Афинность и авидность антител
Сила связывания антител может быть охарактеризована иммунохимическими характеристиками: авидностью и аффинностью.
Под аффинностью понимают силу связывания активного центра молекулы антитела с соответствующей детерминантой антигена. Силу химической связи одного антигенного эпитопа с одним из активных центров молекулы Ig называют аффинностью связи антитела с антигеном. Аффинность количественно принято оценивать по константе диссоциации (в моль-1) одного антигенного эпитопа с одним активным центром.
Аффинность – это точность совпадения пространственной конфигурации активного центра (паратопа) антитела и антигенной детерминанты (эпитопа). Чем больше образуется связей между эпитопом и паратопом, тем выше будут устойчивость и продолжительность жизни образовавшегося иммунного комплекса. Иммунный комплекс, образованный низкоаффинными антителами, чрезвычайно неустойчив и имеет малую продолжительность существования.
Сродство антител к антигену называется авидностью антител. Авидностью связи антитела с антигеном называют суммарную силу прочности и интенсивности связи цельной молекулы антитела со всеми ангитегнными эпитопами, которые ей удалось связать.
Авидность антител характеризуется скоростью образования комплекса «антиген-антитело», полнотой взаимодействия и прочностью образующегося комплекса. В основе авидности, так же, как и в основе специфичности антител, лежит первичное строение детерминанты (активного центра) антитела и связанная с ней степень адаптации поверхностной конфигурации полипептидов антител к детерминанте (эпитопу) антигена.
Авидность определяется как аффинностью взаимодействия между эпитопами и паратопами, так и валентностью антител и антигена. Авидность зависит от числа антигенсвязывающих центров в молекуле антитела и их способностью связываться с многочисленными эпитопами данного антигена.
Типичная молекула IgG при вовлечении в реакцию обоих антиген-связывающих участков будет связываться с мультивалентным антигеном по меньшей мере в 10000 раз сильнее, чем в том случае, когда воэлечен лишь один участок.
Наибольшей авидностью обладают антитела класса М, так как они имеют 10 антигенсвязывающих центров. Если сродство отдельных антиген-связывающих участков IgG и IgM одинаково, молекула IgM (имеющая 10 таких участков) проявит несравненно большую авидностъ к мультивалентному антигену, чем молекула IgG (имеющая 2 участка). Благодаря высокой общей авидности антитела IgM — основной класс иммуноглобулинов, вырабатываемых в начале иммунного ответа, — могут эффективно функционировать даже при низком сродстве отдельных связывающих участков.
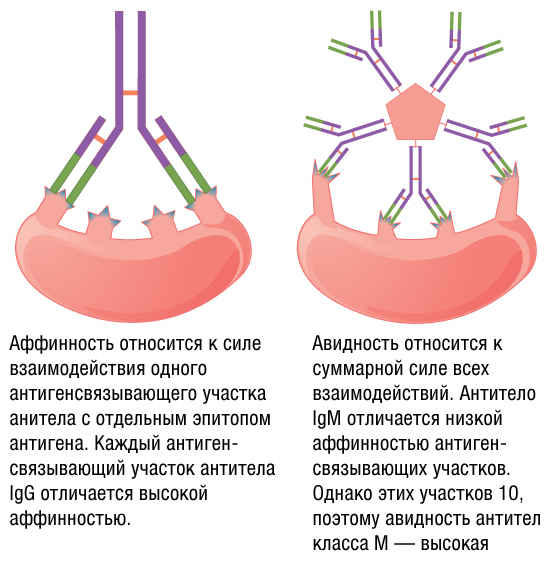
Различие в авидиости весьма важно, так как антитела, образующиеся на ранних стадиях имунного ответа, обычно обладают значительно меньшим сродством к антигену, чем те, которые вырабатываются позже. Повышение среднего сродства продуцируемых антител с течением времени после иммунизации называется созреванием сродства.
Специфичность взаимодействия антигенов и антител
В иммунологии под специфичностью понимают избирательность взаимодействия индукторов и продуктов иммунных процессов, в частности, антигенов и антител.
Специфичность взаимодействия для антител — это способность иммуноглобулина реагировать только с определенным антигеном, а именно — способность связываться со строго определенной антигенной детерминантой. Феномен специфичности основан на наличии активных центров в молекуле антител, вступающих в контакт с соответствующими детерминантами антигена. Избирательность взаимодействия обусловлена комплементарностью между структурой активного центра антитела (паратопа) и структурой антигенной детерминанты (эпитопа).
Специфичностью антигена называют способность антигена индуцировать иммунный ответ к строго определенному эпитопу. Специфичность антигена во многом определяется свойствами составляющих его эпитопов.
Иммунные комплексы
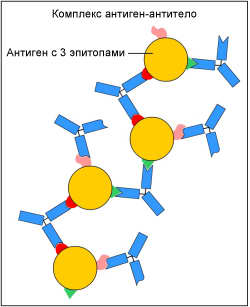
Одной из важнейших функций иммуноглобулинов является связывание антигена и образование иммунных комплексов. Белки-антитела специфически реагируют с антигенами, образуя иммунные комплексы — комплексы антител, связанных с антигенами. Такая связь отличается неустойчивостью: образовавшийся иммунный комплекс (ИК) может легко распадаться на составляющие его компоненты.
К каждой молекуле антигена может присоединиться несколько молекул антител, поскольку на антигене есть несколько антигенных детерминант и к каждой из них могут образовываться антитела. В результате возникают сложные молекулярные комплексы.
Образование иммунных комплексов является неотъемлемым компонентом нормального иммунного ответа. Формирование и биологическая активность иммунных комплексов зависят, в первую очередь, от природы антител и антигена, входящих в их состав, а также от их соотношения. Особенности иммунных комплексов зависят от свойств антител (валентность, аффинность, скорость синтеза, способность связывать комплемент) и антигена (растворимость, размер, заряд, валентность, пространственное распределение и плотность эпитопов).
Взаимодействие антигенов и антител. Реакция антиген-антитело
Реакция антиген-антитело — образование комплекса между антигеном и направленными к нему антителами. Изучение таких реакций имеет большое значение для понимания механизма специфического взаимодействия биологических макромолекул и для выяснения механизма серологических реакций.
Эффективность взаимодействия антитела с антигеном существенно зависит от условий, в которых происходит реакция, прежде всего от pH среды, осмотической плотности, солевого состава и температура среды. Оптимальными для реакции антиген-антитело являются физиологические условия внутренней среды макроорганизма: близкая к нейтральной реакция среды, присутствие фосфат-, карбонат-, хлорид- и ацетат-ионов, осмолярность физиологического раствора (концентрация раствора 0,15 М), а также температура 36-37 °С.
Взаимодействие молекулы антигена с антителом или его активным Fab-фрагментом сопровождается изменениями пространственной структуры молекулы антигена.
Поскольку при соединении антигена с антителом не возникает химических связей, прочность этого соединения определяется пространственной точностью (специфичностью) взаимодействующих участков двух молекул — активного центра иммуноглобулина и антигенной детерминанты. Мера прочности связи определяется афинностью антитела (величиной связи одного антигенсвязывающего центра с индивидуальным эпитопом антигена) и его авидностью (суммарной силой взаимодействия антитела с антигеном в случае взаимодействия поливалентного антитела с поливалентным антигеном).
Все реакции антиген-антитело обратимы; комплекс "антиген-антитело" может диссоциировать с выделением антител. При этом обратная реакция антиген—антитело протекает значительно медленнее, чем прямая.
Можно выделить два основных пути, с помощью которых может быть частично или полностью разделен уже сформировавшийся комплекс антиген — антитело. Первый состоит в вытеснении антител избытком антигена, а второй — в воздействии на иммунный комплекс внешних факторов, приводящих к разрыву связей (уменьшению сродства) между антигеном и антителом. Частичная диссоциация комплекса "антиген—антитело" может быть достигнута в общем случае при повышении температуры.
При использовании серологических методов наиболее универсальным способом диссоциации иммунных комплексов, образованных самыми разнообразными антителами, служит их обработка разбавленными кислотами и щелочами, а также концентрированными растворами амидов (мочевины, солянокислого гуанидина).
Гетерогенность антител
Антитела, образовавшиеся при иммунном ответе организма, неоднородны и отличаются друг от друга, т.е. они гетерогенны. Антитела гетерогенны по своим физико-химическим, биологическим свойствам и прежде всего по своей специфичности. Главная основа гетерогенности (разнообразия специфичностей) антител — разнообразие их активных центров. Последняя связана с вариабельностью аминокислотного состава в V-областях молекулы антитела.
Также антитела гетерогенны по принадлежности к различным классам и подклассам.
Гетерогенность антител связана также с тем, что иммуноглобулины содержат 3 вида антигенных детерминант: изотипические, характеризующие принадлежность иммуноглобулина к определенному классу; аллотипические, соответствующие аллельным вариантам иммуноглобулина; идиотипические, отражающие индивидуальные особенности иммуноглобулина. Система идиотип−антиидиотип составляет основу так называемой сетевой теории Ерне.
Изотипы, аллотипы, идиотипы антител
Иммуноглобулины содержат три вида антигенных детерминант: изотипические (одинаковые для каждого представителя данного вида), аллотипические (детерминанты, различные у представителей данного вида) и идиотипические (детерминанты, определяющие индивидуальность данного иммуноглобулина и являющиеся различными у антител одного класса, подкласса).
У каждого биологического вида тяжелые и легкие цепи иммуноглобулинов имеют определенные антигенные особенности, в соответствии с которыми тяжелые цепи разделены на 5 классов (γ, μ, α, δ, ε ), а легкие на 2 типа (κ и λ). Эти антигенные детерминанты называют изотипическими (изотипы), для каждой цепи они одинаковые у каждого представителя данного биологического вида.
Вместе с тем имеются внутривидовые различия названных цепей иммуноглобулинов - аллотипы, обусловленные генетическими особенностями организма-продуцента: их признаки генетически детерминированы. Например, у тяжелых цепей описано более 20 аллотипов.
Даже тогда, когда антитела к конкретному антигену относятся к одному классу, подклассу и даже аллотипу, они характеризуются специфическими отличиями друг от друга. Эти различия названы идиотипами. Они характеризуют «индивидуальность» данного иммуноглобулина в зависимости от специфичности антигена-индуктора. Это зависит от особенностей строения V-доменов H- и L- цепей, множества различных вариантов их аминокислотных последовательностей. Все указанные антигенные различия определяются с помощью специфических сывороток.
Классификации антител в соответствии с реакциями, в которых они могут участвовать
Первоначально антитела условно классифицировали по их функциональным свойствам на нейтрализующие, лизирующие и коагулирующие. К нейтрализующим были отнесены антитоксины, антиферменты и вирус-нейтрализующие лизины. К коагулирующим – агглютинины и преципитины; к лизирующим – гемолитические и комплемент-связывающие антитела. С учетом функциональной способности антител были даны названия серологическим реакциям: агглютинация, гемолиз, лизис, преципитация и др.
Исследования антител. Фаговый дисплей.
До недавнего времени изучение антител было затруднено техническими причинами. Иммуноглобулины в организме — это сложная смесь белков. Фракция иммуноглобулинов сыворотки крови представляет собой смесь огромного числа различных антител. Причем относительное содержание каждого вида из них, как правило, очень мало. До недавнего времени, получение чистых антител из иммуноглобулиновой фракции было труднодоступно. Трудность выделения индивидуальных иммуноглобулинов долгое время была препятствием как для их биохимического исследования, так и для установления их первичной структуры.
В последние годы сформировалась новая область иммунологии – инженерия антител, которая занимается получением неприродных иммуноглобулинов с заданными свойствами. Для этого обычно используются два основных направления: биосинтез полноразмерных антител и получение минимальных фрагментов молекулы антител, которые необходимы для эффективного и специфического связывания с антигеном.
Современные технологии получения антител in vitro копируют селекционные стратегии иммунной системы. Одной из таких технологий является фаговый дисплей, который позволяет получать фрагменты антител человека разной специфичности. Гены этих фрагментов могут быть использованы для конструирования полноразмерных антител.
Кроме того, очень часто терапевтические препараты, созданные на основе антител, не требуют привлечения их эффекторных функций посредством Fc-домена, например, при инактивации цитокинов, блокировании рецепторов или нейтрализации вирусов. Поэтому одна из тенденций в конструировании рекомбинантных антител состоит в уменьшении их размера до минимального фрагмента, сохраняющего как связывающую активность, так и специфичность.
Такие фрагменты в некоторых случаях могут быть более предпочтительны из-за их способности лучше проникать в ткани и быстрее выводиться из организма, по сравнению с полноразмерными молекулами антител. Вместе с тем, нужный фрагмент может быть наработан в E.coli или дрожжах, что существенно снижает его стоимость по сравнению с антителами, полученными с использованием культур клеток млекопитающих. К тому же, такой способ наработки позволяет избежать биологической опасности, связанной с применением антител, выделенных из донорской крови.
Миеломные иммуноглобулины
 Белок Бенс-Джонса. Пример молекулы такого иммуноглобулина, который представляет собой димер легких каппа-цепей
Белок Бенс-Джонса. Пример молекулы такого иммуноглобулина, который представляет собой димер легких каппа-цепейТермин иммуноглобулины относится не только к нормальным классам антител, но и к большому числу патологических белков, обычно называемых миеломными белками. Эти белки синтезируются в большом количестве при множественной миеломе, злокачественном заболевании, при котором переродившиеся специфические клетки антителообразующей системы продуцируют большие количества определенных белков, например белки Бенс-Джонса, миеломные глобулины, фрагменты иммуноглобулинов различных классов.
Белки Бенс-Джонса представляют собой либо одиночные κ- или λ-цепи, либо димеры из двух одинаковых цепей, связанных одной дисульфидной связью; они экскретируются с мочой.
Миеломные глобулины содержатся в высокой концентрации в плазме больных множественной миеломой; их Н- и L-цепи имеют уникальную последовательность. Одно время предполагали, что миеломные глобулины представляют собой патологические иммуноглобулины, характерные для опухоли, в которой они образуются, но теперь считают, что каждый из них является одним из индивидуальных иммуноглобулинов, случайно «выбранным» из многих тысяч нормальных антител, образующихся в организме человека.
Установлена полная аминокислотная последовательность нескольких индивидуальных иммуноглобулинов, в том числе миеломных глобулинов, белков Бенс-Джонса, а также легкой и тяжелой цепей одного и того же миеломного иммуноглобулина. В отличие от антител здорового человека все белковые молекулы каждой названной группы имеют одинаковую аминокислотную последовательность и являются одним из многих тысяч возможных антител индивидуума.
Гибридомы и моноклональные антитела
Получение антител для нужд человека начинается с иммунизации животных. После нескольких инъекций антигена (в присутствии стимуляторов иммунного ответа) в сыворотке крови животных накапливаются специфические антитела. Такие сыворотки называются иммунными. Из них специальными методами выделяют антитела.
Однако иммунная система организма животного вырабатывает специальные антитела на огромное множество антигенов. В основе этой способности лежит наличие разнообразия клонов лимфоцитов, каждый из которых вырабатывает антитела одного типа с узкой специфичностью. Общее число клонов у мышей, например, достигает 10^7 –10^10 степени.
Поэтому иммунные сыворотки содержат много молекул антител с различной специфичностью, т. е. имеющих сродство ко многим антигенным детерминантам. Антитела, полученные из иммунных сывороток направлены как против антигена, которым проводилась иммунизация, так и против других антигенов, с которыми встречалось животное-донор.
Для современного иммунохимического анализа и клинического применения очень важны специфичность и стандартизованность применяемых антител. Необходимо получать абсолютно идентичные антитела, что невозможно сделать с помощью иммунных сывороток.
В 1975 году Ж. Кёлер и С. Мильштейн (G. Köhler, C. Milstein) решили эту проблему, предложив метод получения гомогенных антител. Они разработали так называемую «гибридомную технологию» — методику получения клеточных гибридов (гибридом). С помощью этого метода получают гибридные клетки, способные неограниченно размножаться и синтезировать антитела узкой специфичности — моноклональные антитела.
Для получения моноклональных антител производят слияние клеток плазмоцитарной опухоли (плазмоцитомы или множественной миеломы) с клетками селезенки иммунизированного животного, чаще всего мыши. Технология Кёлера и Мильштейна включает в себя несколько этапов.
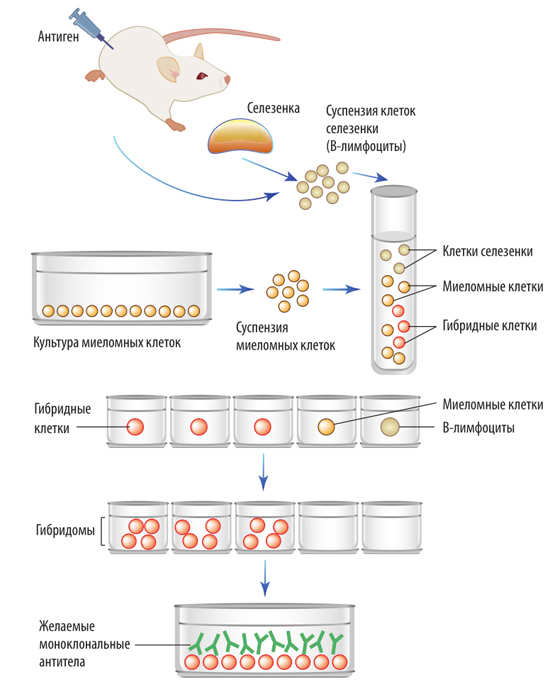
Мыши вводят специфический антиген, который вызывает продукцию антител против этого антигена. Селезенку мышей удаляют и гомогенизируют для получения суспензии клеток. Эта суспензия содержит B-клетки, которые продуцируют антитела против введенного антигена.
Клетки селезенки затем смешивают с клетками миеломы. Это опухолевые клетки, которые способны непрерывно расти в культуре, в них также отсутствует резервный путь синтеза нуклеотидов. Некоторые антителопродуцирующие клетки селезенки и клетки миеломы сливаются, образуя гибридные клетки. Эти гибридные клетки теперь способны непрерывно расти в культуре и продуцировать антитела.
Смесь клеток помещают в селективную среду, которая позволяет расти только гибридным клеткам. Погибают неслившиеся миеломные клетки и В-лимфоциты.
Гибридные клетки пролиферируют, образуя клон гибридом. Гибридомы проверяют на продукцию нужных антител. Выбранные гибридомы затем культивируют для получения больших количеств моноклональных антител, не содержащих посторонних антител и настолько однородных, что могут рассматриваться как чистые химические реагенты.
Следует отметить, что антитела, продуцируемые одной культурой гибридом, связываются только с одной антигенной детерминантой (эпитопом). В связи с этим к антигену с несколькими эпитопами можно получить столько моноклональных антител, сколько у него имеется антигенных детерминант. Также можно отобрать клоны, продуцирующие антитела только одной нужной специфичности.
Разработка технологии получения гибридом имела революционное значение в иммунологии, молекулярной биологии и медицине. Она позволила создать совершенно новые научные направления. Благодаря гибридомам открылись новые пути для изучения и лечения злокачественных опухолей и многих других заболеваний.
В настоящее время гибридомы стали основным источником моноклональных антител, использующихся в фундаментальных исследованиях и в биотехнологии при создании тест-систем. Моноклональные антитела получили широкое распространение при диагностике инфекционных болезней сельскохозяйственных животных и человека.
Благодаря моноклональным антителам стали рутинными иммуноферментный анализ, реакция иммунофлюоресценции, методы проточной цитометрии, иммунохроматографии, радиоиммунный анализ.
Разработано множество технологий, позволивших усовершенствовать синтез антител. Это — технологии рекомбинации ДНК, методы клонирования клеток и другие трансгенные технологий. В 90-х годах, с помощью методов генной инженерии удалось свести к минимуму процент мышиных последовательностей аминокислот в искусственно синтезируемых антителах. Благодаря этому, помимо мышиных, были получены химерные, гуманизированные и полностью человеческие антитела.
Производство моноклональных антител является наиболее быстро развивающимся сегментом фармацевтической индустрии. Развитие биотехнологий позволило создать на основе моноклональных антител лекарства для лечения ряда онкологических, сердечно-сосудистых, инфекционных и аутоиммунных заболеваний, большинство из которых еще несколько десятков лет назад считались неизлечимыми.
запись по телефону 8 (985) 970-30-92 ежедневно с 7.00 до 23.00
ПРИЕМ ТОЛЬКО ПО ЗАПИСИ! ЗВОНИТЕ.
Медицинский центр "На Ленинском" - ежедневно. ЗАПИСЬ!
Медицинский центр "На Самотечной" - cуббота, воскресенье.
По предварительной записи!



